https://doi.org/10.1038/s41467-025-67400-5

Область научных интересов: нейроэтология, нейробиология, нейротрансмиттеры, поведение.
В самом начале 2026-го в журнале «Nature communication» вышла статья исследователей из Израиля, которую можно считать настоящим событием в биологии. В этой работе получены свидетельства того, что эволюция сна предшествует появлению мозга. Поведенческие проявления сон-подобного состояния у двух видов книдарий говорят о том, что многоклеточные организмы выработали эту стратегию, когда их нервная система была представлена еще только элементарной сетью взаимодействующих нейронов. Но основная красота работы заключается в доказательстве того, что сон служит критически важным механизмом для восстановления ДНК нейронов, поврежденной в периоды бодрствования. То есть, сон это проявление заботы о стабильности генома нейронов у самых разных организмов от книдарий до человека. Последний вывод является, конечно, наиболее интересным, он подтверждает относительно недавно появившуюся теорию сна как создание физиологических и молекулярных условий для репарации хрупкой нейрональной ДНК (Zada et al., 2019, 2021). Действительно, такой взгляд хорошо бы объяснял биологический смысл появления сна в эволюции — самого уязвимого поведенческого состояния, распространенного среди животных, имеющих нервную систему. Ради чего этот риск и почему он так распространен? Все предыдущие теории сна не касались настолько существенной для выживания функции как поддержание стабильности генома в нейронах. Эти неделящиеся и высокодифференцированные клетки управляют поведением в зависимости от внешних условий и внутреннего состояния организма, а в соответствии с некоторыми данными и представлениями, именно от состояния нейронов зависит продолжительность жизни всего организма (Оловников 2003; Zullo et al., 2019; Dyakonova 2020).
Не удивительно, что эта новая теория сна появилась относительно недавно, ведь, сам факт, что ДНК в нейронах рвется при обычной поведенческой или сенсорной активности, был впервые установлен только в 2013 году. У мышей после двух часов активности в открытом поле были обнаружены множественные двуцепочечные разрывы ДНК в гиппокампе и других областях мозга (Suberbielle et al., 2013). Уже тогда было замечено, что на следующие сутки большинство этих разрывов репарируется, но предположение о ключевой роли сна в этом процессе высказано не было. Прорыв в ее понимании произошел благодаря статьям 2016-2019 года. В работе (Bellesi et al., 2016), скромно опубликованной в Sci Rep, впервые была показана более активная репарация двуцепочечных разрывов ДНК в нейронах во время сна у мышей и дрозофил. Громче и убедительнее этот вывод прозвучал в 2019 году в работе, посвященной исследованиям сна на мальках рыбы (Zada et al., 2019). В ней прямо показано, что активная динамика хромосом необходима для репарации ДНК, наблюдается в периоды выключенной электрической активности нейронов, а эти периоды, в свою очередь, соответствуют поведенческим периодам сна на уровне организма. Депривация от сна увеличивает число повреждений ДНК в нейронах, и наоборот, увеличение числа разрывов ДНК активирует сон.
Последующее изучение «хрупкости нейрональной ДНК» связано с обнаружением того, что двуцепочечные разрывы ДНК и их последующая репарация необходимы для формирования памяти (Konopka et al., 2022; Navabpour et la., 2020; Weber et al., 2020). К 2024 году уже можно было говорить о появлении новой молекулярной парадигмы памяти на уровне ДНК: «порвал, репарировал, запомнил». Получены экспериментальные доказательства того, что нарушение одного из двух процессов (разрыва или репарации ДНК) нарушает и формирование долговременной памяти. Интересно, что параллельно в отдельной области накапливаются данные о связи сна и консолидации памяти (например, Donlea 2019). Однако, несмотря на интуитивно понятную логику – сон важен для репарации ДНК, которая, в свою очередь, необходима для формирования памяти, и поэтому сон улучшает память – убедительные доказательства этой цепочки пока не представлены. Возможно потому, что ее отдельные звенья пока «прозванивались» по отдельности в разных областях нейробиологии.
Группа под руководством Лиора Аппельбаума (Lior Appelbaum) проверяла гипотезу, что сон является фундаментальным адаптивным решением проблемы мутагенных издержек бодрствования у всех организмов, обладающих нервной системой. Ведь бодрствование характеризуется непрерывным поступлением сенсорной информации, двигательной активностью, усиленным клеточным метаболизмом и электрической активностью нейронов, а все это, как уже сегодня известно, ведет к повреждениям нейрональной ДНК (Дьяконова 2023). Для выстраивания доказательства всеобщности этой роли сна его коллеги использовали представителей двух групп книдарий. Очень элегантный шаг того же коллектива, который ранее показал связь между репарацией ДНК в нейронах и сном у мальков рыбы. В случае большого открытия, сделанного на определенной группе животных, традиционным направлением следующего исследования является смещение в сторону человека. Ведь, до сих пор в глазах общественности наука может быть оправдана только увеличением продолжительности и комфорта жизни человека. И, действительно, небольшой шажок в этом направлении был сделан и этими исследователями, показавшими в 2021 году справедливость своих выводов, сделанных на рыбе, и для теплокровного родственника человека - мыши. Но дальше произошел неожиданный головокружительный разворот к самым примитивным животным. И не просто к хорошо известным модельным беспозвоночным, детально исследованным моллюскам, дрозофиле, модели всех моделей нематоде C. elegans, а к самым простым и малоизученным многоклеточным с нейронами, не собранными даже в ганглии.
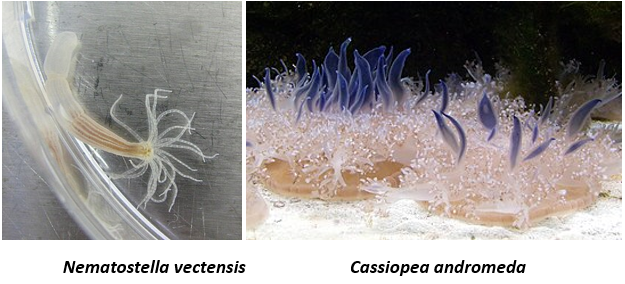
Ранее похожие на сон состояния были задокументированы у H. Vulgaris (Kanaya et al., 2020), а периодическое «поведенческое спокойствие» наблюдалось у кораллов и кубомедуз в их естественной среде обитания (Seymour, et al., 2004; Garmet al., 2012; Kremien et al., 2013). Здесь авторы детально охарактеризовали архитектуру сна сцифоидной медузы C. andromeda и актинии N. vectensis, используя общепринятые поведенческие критерии сна, такие как снижение общей активности, повышение порогов реакций на сенсорные раздражители и наличие ребаунда (отдачи) после депривации от сна. Также, как и у всех организмов, у книдарий во время сна не происходило полное выключение ритмической активности, а наблюдалось только увеличение периода ритма, т.е. снижение частоты сокращений. Авторы обнаружили, что при достижении определенного уровня этой частоты эндогенного ритма происходит значимое изменение чувствительности животных к внешним раздражителям. Для каждого вида были установлены его специфические характеристики. Периоды, характеризующиеся снижением частоты ритма и повышением порогов реакций одновременно, были охарактеризованы как сон. Показано также, что прерывание такого сна или удержание от сна при помощи сенсорной стимуляции вызывает увеличение его длительности после прекращения стимуляции, то есть классический ребаунд после депривации от сна. Было обнаружено, что, как и люди, медуза и актиния нуждаются примерно в 8 часах сна в сутки. Однако спят эти животные в разное время, и также по-разному регулируется у них цикличность сна. C. andromeda характеризуется дневной, а актиния N. vectensis сумеречной активностью. Соответственно, длительные периоды сна у C. andromeda проявлялись в ночное время и более короткие во время дневной сиесты, а у N. vectensis днем.
Сон регулируется освещенностью у C. andromeda, что может объясняться ее симбиозом с фотосинтезирующими динофлагеллятами. Зависимая от освещения фотосинтетическая активность этих симбиотических водорослей может быть использована книдарией для отслеживания циклических изменений освещенности и стать драйвером циклов сна и бодрствования. В отличие от C. andromeda, сумеречная актиния N. vectensis регулирует сон независимо от освещенности на основе внутренних циркадных ритмов. Анализу этих циркадных ритмов посвящен значительный раздел работы, однако в целом, их механизмы остаются все еще малоизученными. Таким образом, выбранные представители книдарий существенно отличаются и суточной ритмикой сна, и механизмами ее регуляции. Эта несхожесть усилила убедительность главного тезиса авторов о роли сна в репарации ДНК в нейронах, поскольку внесла дополнительный сравнительный аргумент в структуру доказательства.
Итак, какие основные экспериментальные доказательства были получены. Во-первых, авторы показали, что число разрывов ДНК в нейронах (оцениваемое иммуногистохимически на основе метки фосфорилированных гистонов γH2AX) коррелирует именно с периодами сна-бодрствования, а не с суточным световым циклом. Красивы противофазные колебания числа разрывов ДНК у двух видов: их снижение в конце темного периода (после сна) у дневной C. andromeda и, наоборот, их повышение у сумеречной N. vectensis, для которой это время соответствует завершению периода бодрствования. Несмотря на различия в хронотипе, сон у обоих видов снижал уровень повреждения ДНК, который повышается во время бодрствования, у обоих видов.
Кроме анализа корреляций с естественным сном, авторы нашли, что мелатонин вызывает сон-подобное состояние у обоих видов, что само по себе является существенным дополнением к ранее полученным данным о консерватизме этой молекулы в регуляции сна у позвоночных и беспозвоночных. Здесь впервые показано, что этот консерватизм можно проследить вплоть до наиболее просто организованных многоклеточных организмов. Обработка мелатонином, которая способствовала сну во время видоспецифичной активной фазы как у N. vectensis, так и у C. andromeda, также снизила уровень очагов γH2AX у обоих видов. А вот депривация от сна, вызванная сенсорной стимуляцией, приводила, наоборот, к значимому накоплению разрывов ДНК у обоих видов.
Следующим важным доказательством стало выявление двусторонней связи между сном и повреждением ДНК: авторы показали, что индукция повреждений повышает потребность во сне. Повреждения вызывали двумя разными способами, используя ультрафиолетовое (УФ) излучение и фармакологический препарат этопозид.
C. andromeda и N. vectensis подвергали воздействию УФ-лучей (312 нм) в течение разного времени (15 и 60 минут соответственно) в дневное время. Через час после облучения у обоих видов наблюдалось увеличение маркеров повреждения ДНК (очагов γH2AX). В ответ на это, C. andromeda стали больше спать днем и ночью, а N. vectensis – только днем. Важно, что после восстановления сна животные выжили, а через два дня уровень повреждения ДНК у C. andromeda снизился.
Поскольку УФ-излучение может влиять на поведение книдарий по альтернативным путям, исследовали также эффекты другого мутагена – этопозида. В то время как УФ-излучение вызывает окислительный стресс, который повреждает ДНК, этопозид ингибирует фермент топоизомеразу II и стабилизирует образование двуцепочечных разрывов ДНК. Аналогично эффекту УФ-излучения, обработка этопозидом резко увеличила количество очагов γH2AX. Соответственно, увеличилась продолжительность сна в течение следующего дня и ночи, после чего повреждение ДНК уменьшилось. Итак, результаты, действительно, показали двунаправленную связь между сном и повреждением ДНК у ранних форм жизни.
Важно, что эти результаты, полученные на простых нервных системах, сходны с данными, полученные и на других эволюционно далеких группах животных, а также людях. Снижение повреждений ДНК, зависящее от сна, было также отмечено у, мух, рыб и мышей (Bellesi et al.,2016; Zada et al., 2019; 2021), а мелатонин улучшил восстановление окислительных повреждений ДНК у работников ночной смены (Zanif et al., 2025). У нематод (DeBardelebenу et al., 2017), мух (Bellesi et al.,2016), рыб (Zada et al., 2019) и мышей (Zada et al., 2021) в похожих экспериментальных схемах была показана необходимость сна для восстановления после клеточного стресса, вызванного такими факторами, как АФК и УФ-излучение, или применение этопозида.
Полученные данные убедительно показывают, что сон предшествовал в эволюции появлению централизованных нервных систем. От себя хочется добавить, что он не только предшествовал, но и, по-видимому, сделал возможным появление более сложных нервных систем, поскольку уже на первых этапах эволюции нейронов была решена проблема мутационной платы за их электрическую активность и высокую пластичность.
На этом красивом нейробиологическом выводе уже можно было бы поставить точку, если бы не данные клеточной биологии о связи циркадных ритмов с геномной стабильностью в ненейронных культивируемых клетках млекопитающих, а также у грибов и цианобактерий (Pregueiro, et al., 2006; Liao and Rust, 2021; Gamsby, et al., 2009; Oklejewicz, et al. 2008)! Интересно, что более быстрые околочасовые ритмы у ненервных клеточных культур регулируются нейротрансмиттерами и, что особенно интересно, мелатонином (Бродский 2025). Могут ли периоды сниженной метаболической активности во время таких более быстрых ритмов также соответствовать периодам быстрых репараций ДНК во время бодрствования, или их физиологический смысл совершенно отличен от репарационной тематики, остается неизвестным. Как бы то ни было, данные, полученные на ненервных клеточных культурах, позволяют предполагать, что клеточные состояния, подобные сну, могли предшествовать и самой эволюции нейронов, которые в очередной раз заимствовали то полезное, что было наработано еще до их появления. Очевидно, на очереди изучение донервных многоклеточных организмов губок и плакозоа.
Литература
Бродский В. Я. (2025) Стабильность прямых взаимодействий клеток. От делений дробления до старости. ЖОБ, Том 86, № 5. Стр. 338–345
Дьяконова В.Е. (2023)Нестабильная днк нейронов: счетчик продолжительности жизни и драйвер эволюции. Обзор.Биохимия 88(11):2084 – 2100. DOI: 10.31857/S0320972523110052
Оловников А. М. (2003) Редусомная гипотеза старения и контроля биологического времени в индивидуальном развитии, Биохимия, 68, 7-41.
Bellesi,M., Bushey, D., Chini, M., Tononi,G. & Cirelli, C. Contribution of sleep to the repair of neuronal DNA double-strand breaks: evidence from flies and mice. Sci. Rep. 6, 36804 (2016).
DeBardeleben, H. K., Lopes, L. E., Nessel, M. P. & Raizen, D. M. Stress-Induced Sleep After Exposure to Ultraviolet Light Is Promoted by p53 in Caenorhabditis elegans. Genetics 207, 571–582 (2017).
Donlea, J. M. Roles for sleep in memory: insights from the fly. Curr. Opin. Neurobiol. 54, 120–126 (2019).
Dyakonova, V. E. (2020) Neuronal counter of the life span: does it exist? Russ. J. Dev. Biol., 51, 197-200, doi: 10.1134/S1062360420030066.
Gamsby, J. J., Loros, J. J. & Dunlap, J. C. A phylogenetically conserved DNA damage response resets the circadian clock. J. Biol. Rhythms 24, 193–202 (2009).
Garm, A., Bielecki, J., Petie, R. & Nilsson, D.-E. Opposite patterns of diurnal activity in the box jellyfish Tripedalia cystophora and Copula sivickisi. Biol. Bull. 222, 35–45 (2012).
Kanaya, H. J. et al. A sleep-like state in Hydra unravels conserved sleep mechanisms during the evolutionary development of the central nervous system. Sci. Adv. 6, eabb9415 (2020).
Kremien, M., Shavit, U.,Mass, T. & Genin, A. Benefit of pulsation in soft corals. Proc. Natl. Acad. Sci. USA 110, 8978–8983 (2013).
Konopka, A., and Atkin, J. D. (2022) The role of DNA damage in neural plasticity in physiology and neurodegeneration, Front. Cell Neurosci., 16, 836885, doi: 10.3389/fncel.2022.836885.
Liao, Y. & Rust, M. J. The circadian clock ensures successful DNA replication in cyanobacteria. Proc. Nat. Acad. Sci. USA 118, 516118 (2021).
Navabpour, S., Rogers, J., McFadden, T., and Jarome, T. J. (2020) DNA double-strand breaks are a critical regulator of fear memory reconsolidation, Int. J. Mol. Sci., 21, 8995, doi: 10.3390/ijms21238995.
Oklejewicz, M. et al. Phase resetting of the mammalian circadian clock by DNA damage. Curr. Biol. 18, 286–291 (2008).
Pregueiro, A. M., Liu,Q., Baker, C. L.,Dunlap, J. C. & Loros, J. J. The neurospora checkpoint kinase 2: a regulatory link between the circadian and cell cycles. Science 313, 644–649 (2006).
Seymour, J. E., Carrette, T. J. & Sutherland, P. A. Do box jellyfish sleep at night? Med. J. Aust. 181, 707 (2004).
Suberbielle, E., Sanchez, P. E., Kravitz, A. V., Wang, X., Ho, K., Eilertson, K., Devidze, N., Kreitzer, A. C., and Mucke, L. (2013) Physiologic brain activity causes DNA double-strand breaks in neurons, with exacerbation by amyloid-β, Nat. Neurosci., 16, 613-621, doi: 10.1038/nn.3356.
Zada, D., Bronshtein, I., Lerer-Goldshtein, T., Garini, Y., and Appelbaum, L. (2019) Sleep increases chromosome dynamics to enable reduction of accumulating DNA damage in single neurons, Nat. Commun., 10, 895, doi: 10.1038/s41467-019-08806-w.
Zada, D., Sela, Y., Matosevich, N., Monsonego, A., Lerer-Goldshtein, T., Nir, Y., and Appelbaum, L. (2021) Parp1 promotes sleep, which enhances DNA repair in neurons, Mol. Cell., 81, 4979-4993.e7, doi: 10.1016/j.molcel.2021.10.026.
Zanif, U. et al. Melatonin supplementation and oxidative DNA damage repair capacity among night shift workers: a randomized placebo-controlled trial. Occup Environ Med https://doi.org/10. 1136/oemed-2024-109824 (2025).
Zullo, J. M., Drake, D., Aron, L., O'Hern, P., Dhamne, S. C., Davidsohn, N., Mao, C. A., Klein, W. H., Rotenberg, A., Bennett, D. A., Church, G. M., Colaiácovo, M. P., and Yankner, B. A. (2019) Regulation of lifespan by neural excitation and REST, Nature, 574, 359-364, doi: 10.1038/s41586-019-1647-8.
Weber Boutros, S., Unni, V. K., and Raber, J. (2022) An adaptive role for DNA double-strand breaks in hippocampus-dependent learning and memory, Int. J. Mol. Sci., 23, 8352, doi: 10.3390/ijms23158352.
Новость подготовила
© В.Е.Дьяконова г.н.с. доктор биологических наук, профессор РАН.
28.01.2026