https://www.mdpi.com/1422-0067/26/9/4243

Область научных интересов: нейроэтология,нейробиология, нейротрансмиттеры, поведение.
Piwi-взаимодействующие РНК (piRNA) играют ключевую роль в подавлении мобильных генетических элементов (МЭ) у животных двумя основными путями. В ядре комплекс Piwi-piRNA индуцирует образование гетерохроматиновой метки H3K9me3 на гомологичных последовательностях МЭ, а в цитоплазме белки Aub и Ago3 расщепляют транскрипты МЭ, запуская ампфикацию piRNA по механизму "пинг-понг". Основные источники piRNA - специализированные геномные кластеры в гетерохроматиновых регионах. Показано, что любая последовательность в активном piRNA-кластере способна генерировать малые РНК, включаясь в систему сайленсинга. Ключевую роль в закреплении кластеров в ряду поколений играет материнское депонированиеи передача piRNA по женской зародышевой линии.Известно, piRNA способны преобразовывать ранее наивные гомологичные локусы в кластер piRNA. Способность piRNA превращать наивные гомологичные локусы в новые кластеры лежит в основе парамутации у Drosophila — эпигенетического «перепрограммирования» одного аллеля другим без изменения последовательности ДНК. Однако из-за ограниченного числа модельных систем неясно, достаточно ли продукции piRNA для парамутационной конверсии наивных локусов.
Какие факторы запускают de novo формирование кластеров? Подавление инсерций МЭ с помощью piRNA может индуцировать гетерохроматизацию эухроматиновых локусов. Более того, такие инсерции способны инициировать образование двуцепочечных piRNA-кластеров. Эпигенетическое подавление может распространяться с инсерций МЭ на прилегающие области, влияя на экспрессию соседних генов. Таким образом, система piRNA иногда ошибочно нацеливается на кодирующие последовательности, запуская образование кластеров, затрагивающих гены. Показано, что piRNA локуса cdi у D. virilis могут преобразовывать гомологичный наивный аллель, демонстрируя парамутационное поведение.
В этой статье мы расширяем представления о природе генных piRNA и их роли в парамутационном преобразовании гомологичных наивных локусов.
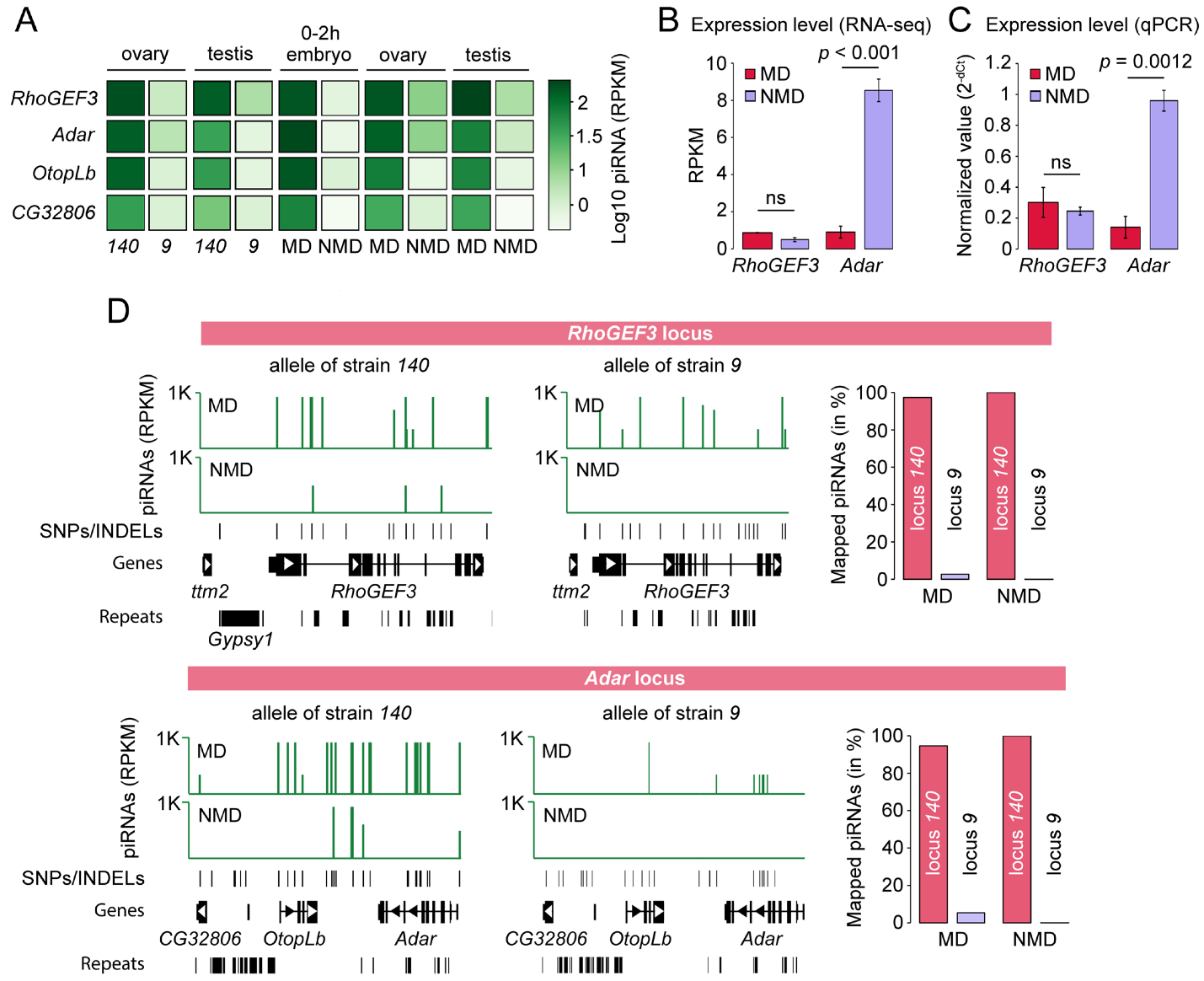
Анализ библиотек малых РНК показал, что гены RhoGEF3, Adar и OtopLb активно продуцируют смысловые и антисмысловые piРНК в гонадах 140 линии D. virilis с признаками канонического биогенеза. Мы установили, что эти локусы функционируют как двуцепочечные piRNA-кластеры в линии 140, но не в линии 9 (Рис.1А). Кластер в локусе Adar охватывает также ген CG32806, а продукция piRNA распределена внутри кластеров неравномерно. Их активность строго коррелирует с обогащением H3K9me3 и приводит к значительному снижению экспрессии гена Adar, но не RhoGEF3, демонстрируя вариабельное влияние piRNA-опосредованного сайленсинга (Рис1В, 1С). Сравнительный анализ геномов выявил ключевое различие — полноразмерную инсерцию ретротранспозона Gypsy1 выше гена RhoGEF3 в линии 140, отсутствующую в линии 9. Gypsy1 — один из наиболее активных МГЭ в D. virilis. Мы предполагаем, что его инсерция и последующий piRNA-опосредованный сайленсинг индуцировали гетерохроматиновое состояние локуса RhoGEF3. В локусе Adar значительных структурных различий не обнаружено, что указывает на роль иных, пока не идентифицированных факторов, хотя наш анализ мог быть ограничен качеством сборки генома.
Рис.1 Материнская передача piРНК запускает их продукцию в потомстве. (А) Влияние материнской передачи piRNA на процессинг piRNA. Экспрессия piRNAs в гонадах 140 и 9 линий, а также у потомства MD (самки 140, скрещенные с самцами 9), которые унаследовали piRNAs, полученные из материнских транскриптов генов и в потомстве NMD (самки 9, скрещенные с самцами 140), которое не унаследовало эти piRNAs. (B, C) Уровни экспрессии генов RhoGEF3 и Adar были определены с помощью RNA-seq и qPCR соответственно. (D) Аллель-специфичное картирование piRNA у реципрокных гибридов. Показаны только те считывания piRNA, которые однозначно сопоставлены с SNP и INDELs, которые различаются между 140 и 9 линиями. Обратите внимание, что ріРНК генерируются из аллеля 9 линии только в потомках MD, но не в NMD. На правой панели показано количество piRNA, картированных на аллели 140 и 9 у потомства MD и NMD, в процентах от общего числа piRNA, картированных на координаты piRNA-кластеров в обеих линиях.
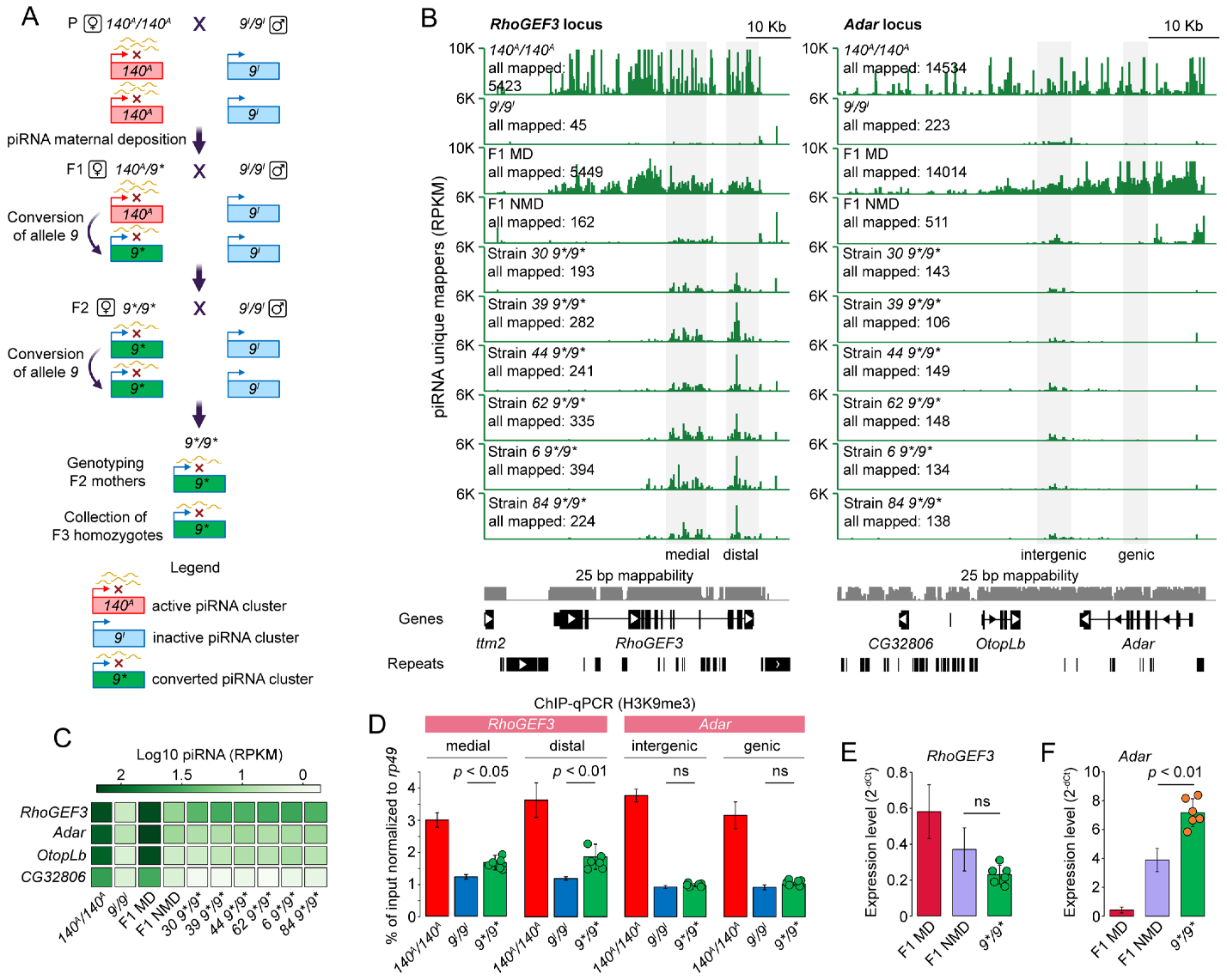
Парамутация у Drosophila инициируется материнской передачей piRNA, активирующей биогенез piRNA на гомологичных локусах in trans. Мы проверили парамутационный потенциал локусов RhoGEF3 и Adar, используя строгую схему скрещиваний для получения потомства (9*/9*), гомозиготного по аллелям линии 9, но ранее экспонированного к материнским piРНК от активных кластеров линии 140 (Рис2А).
Рис2. Проверка парамутагенной активности piРНК-кластеров. (A) Система опосредованного piРНК сайленсинга локусов RhoGEF3 и Adar путем их конверсии в двухцепочечные piРНК-кластеры. Локусы RhoGEF3 и Adar в 140 линии продуцируют piРНК с обеих цепей ДНК. Результаты, представленные в данном исследовании, указывают на то, что матерински унаследованные piРНК, происходящие из обоих локусов 140 линии, способны индуцировать биогенез piРНК с гомологичных аллелей в 9 линии in trans (F1 на рисунке). Парамутация описывает взаимодействие между двумя аллелями локуса, при котором один аллель (парамутагенный аллель) вызывает наследуемые эпигенетические модификации в другом аллеле (парамутируемом аллеле). Модель парамутации у Drosophila характеризуется материнской передачей piРНК, которые усиливают продукцию piРНК из гомологичного локуса. Ключевым моментом является то, что в последующих поколениях биогенез piРНК может поддерживаться с эпигенетически конвертированных локусов (9*/9* на рисунке) в отсутствие исходного запускающего аллеля (140 на рисунке). (B) Профиль покрытия уникально картированных piРНК на локусах RhoGEF3 и Adar (геном D. virilis r.1.06) в яичниках 140 и 9 линий, потомства F1 MD и NMD, а также 9*/9* линий, гомозиготных по аллелям RhoGEF3 и Adar. Показаны все уникально картированные и нормализованные piРНК в данном локусе. Серые области обозначают геномные регионы, которые отличают 9*/9*линии от 9 и NMD в локусе RhoGEF3, а также геномные регионы в локусе Adar, использованные для эксперимента ChIP-qPCR. (C) Экспрессия piРНК, происходящих из транскриптов генов, у родительских штаммов, реципрокных гибридов и потомства, несущего аллели 9*/9* генов RhoGEF3 и Adar. (D) Анализ ChIP-qPCR H3K9me3 в различных регионах локусов RhoGEF3 и Adar в яичниках линий 9*/9*, а также родительских линий 140 и 9. Нормализация по гену rp49. Точки соответствуют значениям для каждой из линий 9*/9*. Статистическая значимость оценивалась с помощью U-критерия Манна-Уитни. Ампликон RhoGEF3 medial соответствует геномной области scaffold_10322:438996-439095, RhoGEF3 distal — scaffold_10322:446114-446273, Adar intergenic — scaffold_12942:65425-65551, Adar gene — scaffold_12942:76684-76817 в геноме D. virilis r.1.06. (E, F) Уровни экспрессии генов RhoGEF3 и Adar, соответственно, в яичниках потомства F1 и потомства, несущего аллели 9*/9* генов RhoGEF3 и Adar. Точки соответствуют значениям для каждой из линий 9*/9*. Для сравнения результатов эксперимента qPCR использовали t-критерий Стьюдента. ns означает незначимо (not significant).
Результаты выявили фундаментальное различие: локус RhoGEF3 демонстрировал устойчивую эпигенетическую память – в поколении F3, без исходного индуцирующего аллеля, сохранялись продукция piRNA и обогащение H3K9me3 (хотя и на сниженном уровне). В отличие от него, локус Adar в этих же условиях полностью утрачивал способность к продукции piRNA, что указывает на зависимость парамутации от хромосомного контекста, а не только от материнских piRNA (Рис.2В).
Ключевым фактором инициации кластера в локусе RhoGEF3, вероятно, стала инсерция ретротранспозона Gypsy1, запустившая каскад событий: сайленсинг транспозона piRNA → распространение гетерохроматиновой метки H3K9me3 → рекрутирование белка Rhino → формирование двуцепочечного кластера. Определенную роль могли сыграть и прилегающие сателлитные повторы pvB370. Для локуса Adar подобные структурные детерминанты не обнаружены.
Проведенные эксперименты предоставили два типа доказательств парамутационно-подобного поведения локуса RhoGEF3. Во-первых, общая экспрессия piRNA к локусу RhoGEF3 у потомства, без исходного парамутагенного аллеля значительно выше, чем у исходного парамутабельного аллеля 9 линии (Рис.2В). Во-вторых, повышенная экспрессия piRNA коррелирует с обогащением H3K9me3 (Рис.2D). Однако, этот эффект оказался локус-специфичным: локус Adar в F3 эту способность утрачивал.
Эффекты piRNA-опосредованной регуляции варьировали: экспрессия Adar подавлялась, а уровень экспресии RhoGEF3 оставался неизменным (Рис.2E, 2F). Расположение парамутагенных локусов в субтеломерных регионах в соседстве с сателлитной ДНК и теломерными ретротранспозонами позволяет предположить, что хромосомный контекст критически важен для парамутации. Эти данные расширяют понимание эпигенетического наследования, показывая, как «ошибки» в защите от транспозонов могут закрепляться как стабильные наследуемые признаки.
Система piRNA — эволюционно консервативный механизм защиты зародышевой линии от МГЭ, чья активность может иметь нецелевые эффекты, приводящие к репрессии генов. В данном исследовании мы изучили образование piRNA из кодирующих генов на примере линий D. virilis, показав, что гены RhoGEF3, Adar, OtopLb и CG32806 служат источником piRNA в линии 140, но не в линии 9. Это предоставляет уникальную модель для изучения эпигенетической конверсии обычных локусов в активные piRNA-кластеры.
Новость подготовил
© с.н.с., к.б.н. Куликова Дина Александровна
26.11.2025