
Область научных интересов: дифференцировка клеток иммунной системы, гемопоэз, регуляция воспаления, инфекционная иммунология.

Область научных интересов: регенеративная медицина, клеточная биология, биоматериалы.
Введение
В 2023 году FDA одобрила первый генно-терапевтический препарат - Экзагамглогенный аутотемцел (Casgevy™; Касгеви), - для лечения бета-талассемии и серповидно-клеточной анемии (серповидно-клеточная болезнь, СКБ, СКА), двух наиболее распространенных генетических заболеваний в мире. Касгеви разработан компаниями Vertex Pharmaceuticals и CRISPR Therapeutics и представляет собой популяцию аутологичных стволовых и прогениторных клеток CD34+, генетически модифицированных ex vivo с помощью системы CRISPR/Cas9 таким образом, чтобы обеспечить выработку фетального гемоглобина.
Бета-талассемия и СКА - β-гемоглобинопатии, в основе которых лежат мутации в гене β-глобина (НВВ), кодирующем одну из цепей, входящих в состав гемоглобина. Гемоглобин – основной компонент эритроцитов, обеспечивающий связывание кислорода и его перенос от легких к тканям, а также выведение углекислого газа. По своему строению гемоглобин является тетрамером, состоящим из 4 цепей. На эмбриональной стадии развития эритроциты содержат т.н. фетальный гемоглобин (HbF), состоящий из двух α-цепей и двух β-подобных γ-глобиновых цепей (α2γ2). В течение полугода после рождения происходит постепенная замена синтеза γ-цепей на синтез β-цепей с образованием т.н. «взрослого» гемоглобина (HbA), состоящего из двух α- и двух β –цепей. В основе механизма замены лежит активность транскрипционных факторов-репрессоров, BCL11A и ZBTB7A, связывающихся с промоторной частью гена γ-глобина и обеспечивающих подавление его транскрипции. (Wang X, Thein SL. Switching from fetal to adult hemoglobin. Nat Genet. 2018 Apr;50(4):478-480. doi: 10.1038/s41588-018-0094-z.)
При СКА в гене β-глобина происходит мутация, приводящая к замене валина на глутамин в 6 положении. Мутация приводит к повышенной склонности гемоглобина к полимеризации и как следствие – к деформации эритроцитов, блокировке мелких кровеносных сосудов и нарушению доставки кислорода в ткани. Клинически отмечаются гемолитические, апластические, секвестрационные кризы, тромбоз сосудов, костно-суставные боли и припухлость конечностей, изменениями скелета, сплено- и гепатомегалия.
При бета-талассемии имеет место либо снижение, либо полное отсутствие экспрессии β-цепи гемоглобина. В результате нарушается баланс между α- и β-цепями гемоглобина, α-цепи накапливаются в избытке, преципитируют на стадии образования предшественников эритроцитов, последние погибают, и развивается анемия. Следствием анемии является усиленное образование новых эритроидных предшественников, гиперплазия эритроидного ростка в костном мозге и экстрамедуллярно, что в конечном итоге приводит к вторичным нарушениям, отмечающимся в костной ткани и других органах (Sankaran VG, Orkin SH. The switch from fetal to adult hemoglobin. Cold Spring Harb Perspect Med. 2013 Jan 1;3(1):a011643. doi: 10.1101/cshperspect.a011643.)
До настоящего времени наиболее доступным методом терапии бета-талассемии и СКА является симптоматическая терапия, заключающаяся в регулярных гемотрансфузиях и хелаторной терапии, что, в свою очередь, может сопровождаться аллергическими и фебрильными реакциями, вызвать осложнения, в частности, синдром острого посттрансфузионного повреждения легких и трансфузионную циркуляторную перегрузку (ТЦП).
Единственной лечебной терапией является трансплантация костного мозга – процедура, которая сама по себе имеет целый ряд серьезных ограничений, связанных, в первую очередь, с трудностями нахождения HLA-совместимого донора и риском развития реакции «трансплантат против хозяина» при иммунологической несовместимости. Касгеви является генно-клеточным препаратом, представляющим собой генетически скорректированные с помощью системы CRISPR/Cas9 аутологичные гемопоэтические стволовые и прогениторные клетки пациента и, таким образом, является прорывом в лечебной терапии гемоглобинопатий.
Принцип работы Касгеви
Принцип, лежащий в основе препарата Касгеви, – увеличение синтеза γ-цепи гемоглобина в аутологичных гемопоэтических клетках. Популяцию аутологичных гемопоэтических стволовых и прогениторных клеток выделяют на основе экспрессии CD34. Полученные клетки CD34+ подвергают генетическому редактированию в области энхансера гена BCL11 таким образом, чтобы снизить связывание транскрипционного фактора GATA1. В результате, в редактированных клетках снижается экспрессия BCL11A, что приводит к повышению экспрессии γ-глобина и продукции в эритроидных клетках HbF. У пациентов с талассемией снижается накопление и преципитация несвязанных α-цепей. У пациентов с тяжелой формой СКА экспрессия фетального гемоглобина снижает уровень внутриклеточного серповидного гемоглобина, тем самым предотвращая серповидность эритроцитов и устраняет болевые кризы.
История разработки Касгеви
В рассматриваемой статье кратко описаны этапы разработки и одобрения Касгеви. В октябре 2015 г. Vertex Pharmaceuticals и CRISPR Therapeutics вошли в коллаборацию по разработке новых методов лечения, основанных на корректировке дефектов специфических генов с использованием технологии CRISPR-Cas9. В апреле 2021 г. Vertex Pharmaceuticals and CRISPR Therapeutics скорректировали договор, включив в него разработку, производство и коммерциализацию экзагамглоген аутотемцела. Доклинические исследования были начаты в марте 2017 г. (Рисунок 1). В 2019 г. в США препарат прошел ускоренный режим одобрения для применения при СКБ (январь 2019) и трансфузионно-зависимой бета-талассемии (апрель 2019 г.). В 2020 г. был разрешен в Евросоюзе для лечения трансфузионно-зависимой талассемии (бета-талассемии) как препарат для лечения орфанных заболеваний. Первое разрешение на применение препарат получил в Великобритании в ноябре 2023 г. для лечения трансфузионно-зависимой бета-талассемии и СКА у пациентов в возрасте ≥ 12 лет, которым показана трансплантация гемопоэтических стволовых клеток (ГСК), но HLA-совместимый донор недоступен. 8 декабря 2023 года Касгеви был одобрен в США для лечения СКА у пациентов в возрасте ≥ 12 лет с рецидивирующими вазоокклюзивными кризами (ВОК), 14 декабря 2023 года получил положительное заключение в ЕС для лечения бета-талассемии и СКА. В настоящее время проводится регуляторная оценка Касгеви для лечения бета-талассемии в США. Основные вехи разработки препарата приведены на Рисунке1.
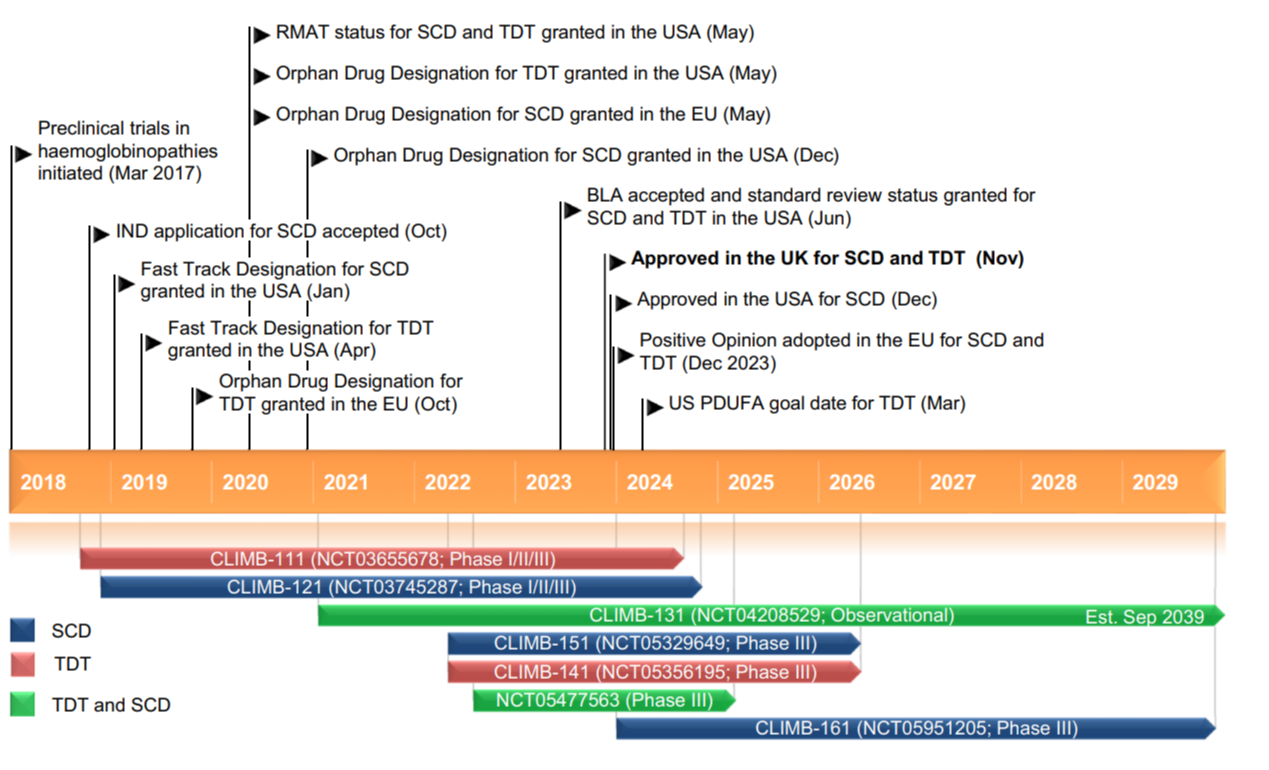
Рисунок 1. Основные этапы разработки Касгеви.
BLA - заявка на получение биологической лицензии, Est - приблизительная оценка, IND -новое исследуемое лекарство, PDUFA - закон о плате за использование рецептурных препаратов, RMAT - передовая терапия (регенеративная медицина), SCD - серповидно-клеточная болезнь (СКБ), TDT - трансфузионно-зависимая β-талассемия (ТЗТ)
Основные характеристики препарата
Класс: антианемический препарат; генная терапия; терапия гемопоэтическими стволовыми клетками; терапия стволовыми клетками.
Механизм действия: замещение клеток, стимуляция экспрессии фетального гемоглобина
Фармакодинамика: существенное увеличение доли аллелей с введенной генетической модификацией
Наиболее частые побочные реакции: лимфопения
АТС код Всемирной организации здравоохранения: B06A-X05
Фармакодинамика
Касгеви эффективно редактирует аллели. По данным авторов статьи, в течение месяца после введения препарата наблюдалось значительное аллельное редактирование как у пациентов с бета-талласемией, так и у пациентов с СКА. Среднее соотношение модифицированных аллелей постоянно увеличивалось, достигало 77,4% и 85,9% соответственно к 6-му месяцу, выходило на плато и оставалось стабильным до 24 месяца.
Касгеви значительно повышает уровень фетального гемоглобина. У пациентов с СКА уровень фетального гемоглобина увеличивался с 36,9 % на 3-м месяце терапии до 42,1 % на 24-м месяце, что способствовало повышению общего уровня гемоглобина. Более того, в соответствии с этим увеличением средняя доля циркулирующих эритроцитов, экспрессирующих фетальный гемоглобин, составила 70,1% на 3-м месяце и 94,0% на 6-м месяце, после чего их уровни оставались стабильными. Статистический анализ подгрупп показал, что влияние терапии на аллельное редактирование, уровень фетального гемоглобина и общего гемоглобина было одинаковым в разных возрастных группах (подростки и взрослые) и полах (мужчины и женщины).
Исследования in vitro с использованием клеток здоровых доноров и пациентов не выявили признаков внецелевого редактирования. Эти данные подчеркивают эффективность и безопасность препарата Касгеви в аллельном редактировании, повышении выработки фетального гемоглобина и улучшении общего уровня гемоглобина у пациентов с бета-талласемией и СКА.
Клинические исследования
Авторы считают результаты клинических исследований Касгеви при лечении бета-талласемии и СКА многообещающими. Однократная инъекция Касгеви показала его эффективность в 24-месячном исследовании I/II/III фазы (CLIMB-111) с участием пациентов в возрасте 12-35 лет с бета-талласемией.
Высокий процент достижения первичного результата: 93% из 42 пациентов, отвечающих критериям отбора, достигли первичного результата - поддержания уровня гемоглобина без необходимости переливания крови в течение, как минимум, 12 месяцев подряд после инфузии.
93,5% из 31 пациента, отвечающего критериям отбора, достигли первичного результата, заключающегося в отсутствии тяжелого вазоокклюзивного криза (ВОК) в течение как минимум 12 месяцев подряд.
Значительное снижение частоты переливания крови: даже у тех пациентов, которые не достигли первичного результата, потребность в переливании крови значительно снизилась.
Значительное снижение тяжелых кризов: у пациентов, достигших первичного результата, наблюдалось значительное снижение частоты и тяжести болевых кризов.
Строгие критерии отбора пациентов: пациенты отбирались с учетом их истории частых переливаний крови, хорошего общего состояния здоровья, отсутствия тяжелой перегрузки железом или прогрессирующих заболевания печени. Для сбора стволовых клеток для редактирования пациентам проводили аферез, затем миелоаблативное кондиционирование перед применением препарата.
Строгие критерии отбора пациентов: пациенты отбирались с учетом частоты и тяжести ЛОС (длительный сосудоокклюзионный криз) в анамнезе, хорошего общего состояния здоровья, отсутствия прогрессирующих заболеваний печени или других специфических состояний.
Побочные эффекты
При сравнении с миелоаблативным кондиционированием и трансплантацией гемопоэтических стволовых клеток Касгеви продемонстрировал профиль безопасности, соответствующий установленным рискам; профиль безопасности не зависел возраста пациента.
Общие нежелательные реакции:
Наиболее распространенной побочной реакцией у пациентов как с бета-талласемией, так и с СКА, была лимфопения. Другие побочные реакции включали мукозит, фебрильную нейтропению, снижение аппетита, нейтропению, тромбоцитопению, лейкопению, анемию и лимфопению и чаще отмечались у пациентов с СКА.
Период повышенного риска кровотечений существует до тех пор, пока не произойдет приживление тромбоцитов, обычно около 44 дней для пациентов с бета-талласемией и 35 дней для пациентов с СКА.
Серьезные нежелательные реакции:
У двух пациентов с бета-талласемией наблюдались серьезные побочные реакции, связанные с Касгеви, включая гемофагоцитарный лимфогистоцитоз, острый респираторный дистресс-синдром, синдром идиопатической пневмонии, головную боль, задержку приживления и тромбоцитопению.
Ни в одной из популяций пациентов не наблюдалось случаев болезни «трансплантат против хозяина», отказа трансплантата или отторжения трансплантата.
Эта информация подчеркивает, что, хотя Касгеви имеет некоторые проблемы с безопасностью, связанные с миелоаблативным кондиционированием и трансплантацией гемопоэтических стволовых клеток, его общий профиль безопасности достаточно благоприятен. Важно отметить, что представленная информация основана на промежуточных данных, и для полного понимания долгосрочной безопасности Касгеви необходим дальнейший долгосрочный мониторинг.