 © Шевелева Ольга Николаевна, научный сотрудник Лаборатории клеточных и молекулярных основ гистогенеза, кандидат биологических наук.
© Шевелева Ольга Николаевна, научный сотрудник Лаборатории клеточных и молекулярных основ гистогенеза, кандидат биологических наук.
В наше время все более актуальной становится проблема бесплодия. Частично она решается благодаря широкому распространению искусственного оплодотворения. Однако зачастую эта дорогостоящая процедура оказывается недостаточно эффективной из-за проблем с имплантацией эмбриона. Имплантация – это комплексный процесс, подразумевающий тесное взаимодействие между стенкой матки матери и эмбрионом на стадии бластоцисты. При этом важную роль играют клетки трофобласта, которые мигрируют и внедряются в стенку матки, обеспечивая прикрепление зародыша и начало образования плаценты. Успешность имплантации и правильное формирование плаценты определяет в дальнейшем успешность всей беременности.
До сих пор подавляющее большинство исследований, посвященных имплантации, сосредотачивались на изучении взаимодействия клеток матки с клетками трофобласта. Работа Desrochers et al, 2016 года посвящена исследованию нового механизма, лежащего в основе успешной имплантации эмбриона, - взаимодействия между клетками внутренней клеточной массы (ВКМ) и трофобласта внутри самого зародыша. Это взаимодействие осуществляется с помощью внеклеточных везикул, секретируемых клетками ВКМ и поглощаемых клетками трофобласта.
Как известно, внеклеточные везикулы (экзосомы и микровезикулы) несут широкий спектр различных белков, микроРНК, мРНК и даже ДНК и выделяются самыми разными типами клеток, участвуя в межклеточных взаимодействиях. В данной работе авторы остановили свое внимание на микровезикулах, продуцируемых эмбриональными стволовыми клетками (ЭСК), которые получают из ВКМ бластоцист.
В первую очередь было изучено действие кондиционированной среды от ЭСК на клетки трофобласта линии HTR8/SVneo и показано, что в отличие от контроля (обычной ростовой среды), инкубация в кондиционированной среде приводила к увеличению количества фосфорилированных (активированных) форм FAK и JNK белков. Миграционный анализ на двухмерной модели экспериментальной раны in vitro показал, что кондиционированная среда от ЭСК стимулировала миграцию клеток трофобласта. При этом ингибирование FAK и JNK блокировало это действие кондиционированной среды.
Выделенные из кондиционированной среды микровезикулы (внеклеточные везикулы размером 350-800 нм, экспрессирующие флотилин-2) индуцировали фосфорилирование FAK и JNK и способствовали миграции клеток трофобласта на модели экспериментальной раны, так же, как кондиционированная среда в целом. А добавление микровезикул к клеткам трофобласта, содержащимся в бессывороточной среде, на 1 час вызывало приобретение этими клетками морфологии и распределения Rac1 и F-актина, характерных для мигрирующих клеток. Вдвое большее число клеток трофобласта, культивируемых в среде с микровезикулами, формировали хорошо различимые «лидирующие края» по сравнению с клетками в обычной среде. Интересно, что такой способностью влиять на миграцию клеток трофобласта обладали только везикулы, полученные от ЭСК, но не от клеток трофобласта линии HTR8/SVneo.
При инкубации бластоцист мыши в среде, содержащей микровезикулы, эмбрионы формировали отростки, причем площадь занимаемая отростками, была, по крайней мере, в три раза больше, чем у бластоцист, содержащихся в обычной среде, без добавления везикул.
Поскольку активация миграции клеток трофобласта в присутствии микровезикул от ЭСК начиналась в течение часа, авторы предположили, что основную роль в этом процессе играют именно белки, содержащиеся в везикулах. Был проведен протеомный анализ и среди 10 наиболее многочисленных белков в составе микровезикул были особо выделены фибронектин и ламинин α5, поскольку есть данные об участии этих белков в имплантации и формировании плаценты. Кроме того, оба этих белка внеклеточного матрикса, связываясь с рецепторами на поверхности клеток трофобласта, запускали сигнальные пути через киназы - FAK и JNK, активируя миграцию этих клеток. Добавление ингибирующих действие фибронектина и ламинина пептидов – RGD и YIGR, соответственно, к клеткам трофобласта, культивируемых в среде с микровезикулами от ЭСК, приводило к элиминации влияния везикул на миграцию этих клеток.
И, наконец, инъекция меченных GFP микровезикул от ЭСК в бластоцисты, показала, что везикулы могут передаваться в клетки трофоэктодермы и увеличивают вероятность имплантации бластоцист при их помещении в матку суррогатных мышей по сравнению с бластоцистами, в которые инъецировалась просто среда без везикул.
Таким образом, Desrochers с коллегами показали, что ЭСК секретируют микровезикулы, содержащие в большом количестве белки внеклеточного матрикса – фибронектин и ламинин α5, которые, взаимодействуя с клетками трофобласта, активируют их миграцию и влияют на имплантацию. Использование таких микровезикул в терапевтических целях в дальнейшем поможет увеличивать вероятность успешной имплантации эмбрионов и способствовать сохранению беременности.
|
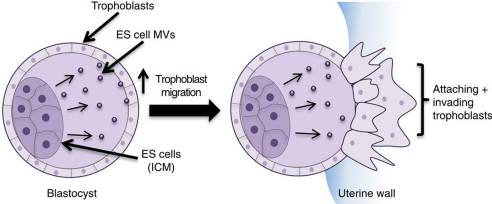
Рис 1. Схема, демонстрирующая способность ЭСК взаимодействовать с клетками трофобласта, содействуя имплантации эмбриона. ЭСК находятся в ВКМ и окружены клетками трофобласта (левое изображение). Наряду с клетками материнского организма, они могут вносить свой вклад в процесс имплантации бластоцисты, генерируя микровезикулы (правое изображение), активирующие сигнальные события в клетках трофобласта.
© Copyright © 2016 Sheveleva O.N.