© Орлова Евгения Алексеевна,, м.н.с. лаборатории эпигенетики развития ИБР РАН.
© Орлова Евгения Алексеевна,, м.н.с. лаборатории эпигенетики развития ИБР РАН. Область научных интересов: клеточная биология, плюрипотентные стволовые клетки человека, механизмы поддержания стабильности генома, клеточное старение, прогероидные синдромы, поддержание теломер в клеточных линиях.
Исследования в области биологии старения человека - стремительно развивающаяся сфера науки. Благодаря различным животным моделям достигнут прогресс в исследовании механизмов старения, однако подобные стратегии не способны отразить биологию старения человека. Индуцированные плюрипотентные стволовые клетки (иПСК), полученные в результате репрограммирования соматических клеток пациентов с синдромами преждевременного старения, представляют собой современную модель для изучения фундаментальных механизмов старения. Считается, что при репрограммировании происходит стирание прогероидных признаков, обновление клеток, а дифференцировка иПСК позволяет проследить инициацию и развитие клеточных и молекулярных проявлений признаков старения. Подобных клеточных моделей у нас в стране нет. Наша лаборатория занимается перепрограммированием фибробластов пациентов с прогероидными синдромами и соответствующих им контролей (клетки здоровых пациентов) в иПСК, а также характеристикой таких клеточных моделей.
Процесс ускоренного старения наиболее подробно изучен для прогерии Хатчинсон-Гилфорда (HGPS), вызванной гетерозиготной мутацией c.1824C>T (p.Gly608Gly) в гене LMNA, кодирующем ламин А. Репрограммирование фибробластов пациента с HGPS приводит к их обновлению за счет снижения экспрессии мутантного ламина А, прогерина, в стволовых клетках. Неонатальный прогероидный синдром Видемана-Раутенштрауха (WRS) отличается наиболее ранним появлением признаков преждевременного старения и вызван компаунд-гетерозиготной мутацией c.3337-11T>C/c.3677T>C в гене POLR3A, кодирующем каталитическую субъединицу РНК-полимеразы III, которая принимает участие в регуляции продолжительности жизни модельных животных.
Благодаря применению неинтегративного метода репрограммирования нами были получены иПСК из фибробластов пациентов с синдромами HGPS и WRS и соответствующих им контролей. Модель из клеток пациента с WRS была разработана и охарактеризована впервые в мире. Результаты нашей исследовательской работы опубликованы в журнале Biogerontology.
С целью характеристики объектов исследования, а именно, исходных фибробластов, было проведено окрашивание на ассоциированную с сенесцентностью активность бета-галактозидазы и проанализирована экспрессия ингибиторов клеточного цикла. В фибробластах пациентов с HGPS и WRS наблюдалась повышенная активность лизосомальной бета-галактозидазы уже на ранних пассажах. Уровни ингибиторов клеточного цикла p16 и p21 были также повышены в фибробластах HGPS (пассаж 12) и фибробластах WRS (пассаж 20) по сравнению с контрольными клетками. При переходе в плюрипотентное состояние экспрессия этих маркеров старения отсутствовала.
В процессе исследования было установлено, что патогенные мутации, ассоциированные с генами данных синдромов, не влияли на процесс репрограммирования и поддержания плюрипотентности полученных линий иПСК. В этих линиях выявлена экспрессия факторов плюрипотентности (NANOG, SOX2, OCT4) и ДНК-метилтрансферазы 3b (DNMT3B), а также отмечена активация экспрессии энзиматического компонента теломеразы TERT по сравнению с фибробластами.
Кроме того, плюрипотентность каждой линии иПСК подтверждали по способности дифференцироваться в производные трёх зародышевых листков благодаря проведению спонтанной дифференцировки in vitro. Эмбриоидные тельца были успешно сформированы исследуемыми линиями иПСК и содержали клетки, экспрессирующие маркеры эктодермы (OTX2, SOX2), мезодермы (Desmin, αSMA) и энтодермы (SOX17), что подтверждает истинную плюрипотентность полученных линий. При проведении эксперимента по дифференцировке данных иПСК in vivo с использованием тератомного теста на иммунодефицитных мышах было установлено, что все клоны также способны к образованию тератом, которые, в свою очередь, содержат ткани из трёх зародышевых листков, включая эктодерму, мезодерму и энтодерму.
Один из основных результатов исследования заключается в том, что иПСК HGPS и WRS продемонстрировали разную степень проявления мутантного фенотипа. В фибробластах HGPS наблюдался высокий уровень прогерина, что приводит к проявлению признаков старения на клеточном уровне. Однако после репрограммирования в иПСК HGPS прогерин практически не детектировался, что связано с отсутствием экспрессии ламина А и его токсичной формы в плюрипотентных клетках в целом. Это объясняет отсутствие прогероидных признаков в этих клетках.
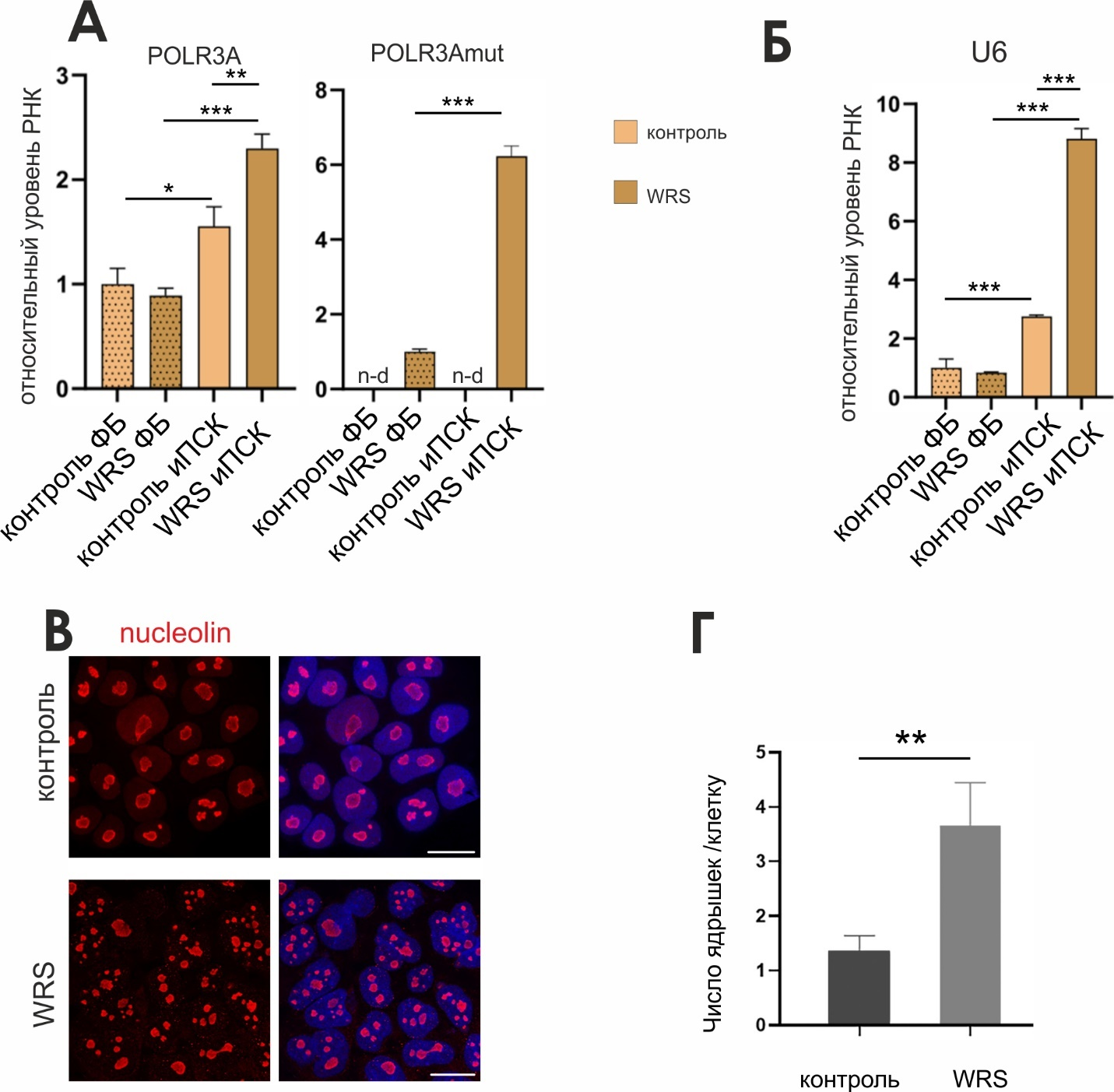
В отличие от ламина А, при репрограммировании в норме происходит повышение уровня мРНК POLR3A в контрольных иПСК. Вместе с этим экспрессия POLR3A в иПСК WRS ещё более повышена по сравнению с контрольными клетками. Используя праймеры, специфичные к мутантной мРНК c.3677T>C POLR3A, мы продемонстрировали накопление этих транскриптов в иПСК WRS по сравнению с фибробластами (Рис. 1А). Более того, достоверно повышался уровень экспрессии одной из ключевых малых ядерных РНК, U6, транскрибируемой РНК полимеразой III (Рис. 1Б). Это означает, что при репрограммировании не происходит обновления прогероидных клеток.
Высокий уровень мутантного POLR3A может оказывать негативное влияние на клеточный метаболизм в стволовых клетках WRS. Нарушение регуляции экспрессии генов, опосредованной Pol III, способно привести к патологиям функционирования ядрышка. С помощью иммуноокрашивания антителами к нуклеолину, компоненту внешнего гранулярного компонента ядрышка, нами показано, что клетки иПСК WRS имеют значительно большее число ядрышек на клетку и демонстрируют их аномальную сегментированную структуру по сравнению с контрольными иПСК (Рис. 1В, Г). Таким образом, мутация POLR3A приводит к нарушению регуляции РНК U6, продуцируемой полимеразой III, что сопровождается дефектами в количестве и морфологии ядрышек в иПСК WRS.
Рис. 1. В линии иПСК от пациента с синдромом Видемана-Раутенштрауха (WRS) наблюдается высокий уровень экспрессии мутантного POLR3A и нарушение структуры ядрышка. (А) ОТ-кПЦР анализ экспрессии POLR3A в контрольных и полученных от пациента WRS фибробластах и соответствующих линиях иПСК. Планки погрешностей указывают SEM, n=4 (* P < 0,05–0,01, ** P < 0,01–0,001, ***P < 0,001, непарный t-тест). n-d — не обнаружено. (Б) ОТ-кПЦР-анализ экспрессии 6U в контрольных и полученных от пациента WRS линиях иПСК. Планки погрешностей указывают стандартную ошибку среднего (SEM), n=4 (* P < 0,05–0,01, ** P < 0,01–0,001, ***P < 0,001, непарный t-критерий). (В) Иммуноокрашивание нуклеолина выявляет изменения количества и морфологии ядрышек в иПСК WRS. Показаны репрезентативные изображения фрагментов колоний иПСК. ДНК окрашена DAPI. Шкала 20 мкМ. (Г) Представлена количественная оценка количества ядрышек в контрольных и полученных от пациентов с WRS иПСК. Планки погрешностей указывают стандартную ошибку среднего (SEM) для четырех независимых экспериментов (количество клеток > 200), ** P < 0,01–0,001, непарный двусторонний t-критерий (Orlova et al., 2025; разрешение предоставлено издательством Springer Nature, номер лицензии 6161991081406).
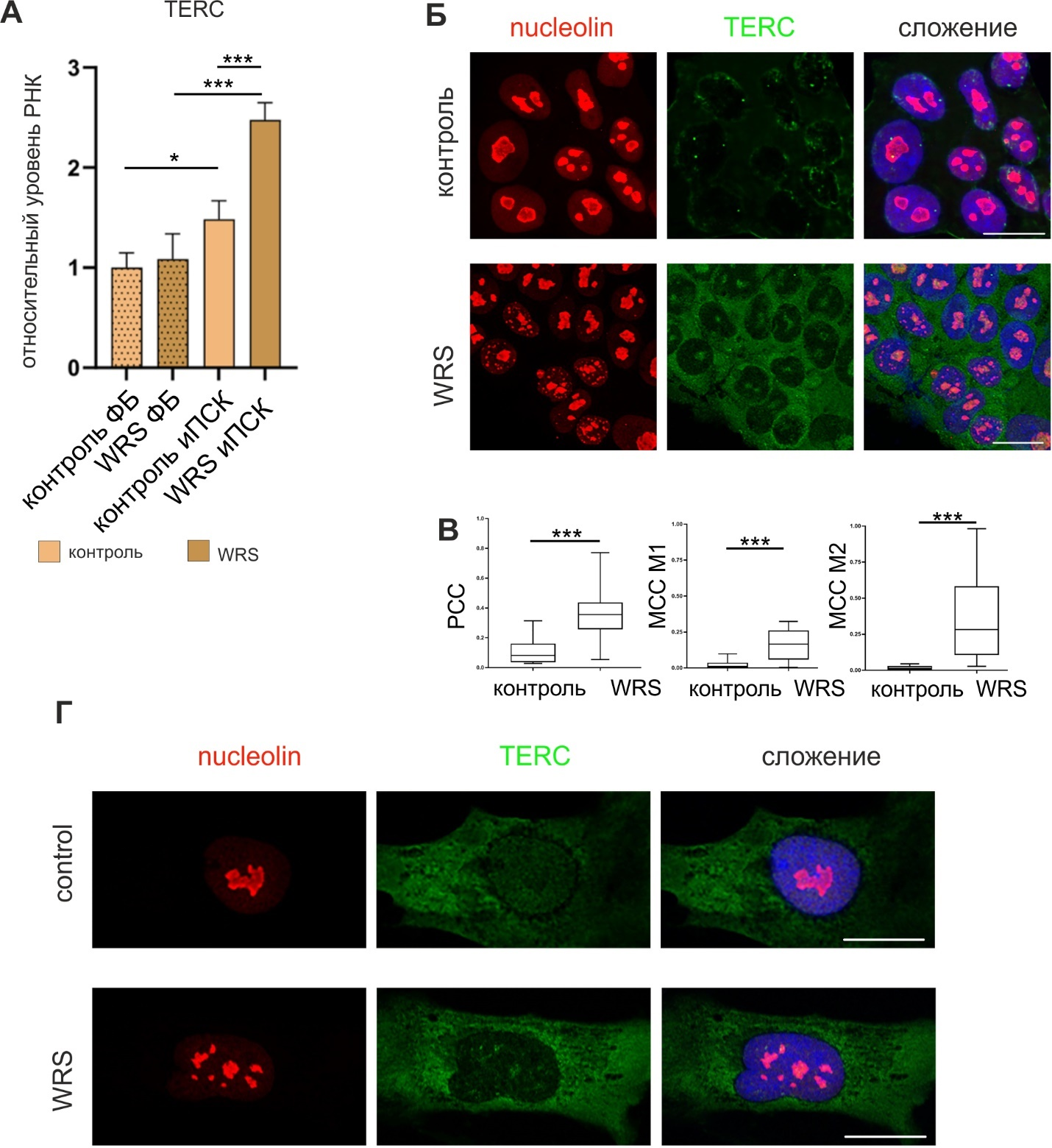
Переход клеток в состояние плюрипотентности сопровождается активацией теломеразы и удлинением теломер, что обеспечивает геномную стабильность стволовых клеток. В ходе исследования нами было установлено, что в иПСК пациентов с WRS происходит нарушение биогенеза теломеразной РНК (TERC), вызывая задержку TERC в ядрышках. В иПСК в норме наблюдается незначительное повышение уровня экспрессии теломеразной РНК (TERC) по сравнению с фибробластами, но уровень экспрессии TERC значительно выше в иПСК WRS по сравнению с контрольными иПСК (Рис. 2А). В результате комбинирования методов флуоресцентной гибридизации in situ с зондом, детектирующим TERC, и иммуноокрашивания антителами к нуклеолину было установлено, что TERC накапливается в ядрышках иПСК WRS, частично перекрываясь с сигналами нуклеолина, и локализован в фокусах нуклеоплазмы в контрольных иПСК (Рис. 2Б) Статистический анализ колокализации подтвердил сильное обогащение TERC в ядрышках в иПСК WRS (Рис. 2В). Аномальные сегментированные ядрышки со слабыми сигналами TERC также наблюдались в фибробластах WRS (на 13 пассаже), что указывает на схожие патологические проявления как в дифференцированных, так и в стволовых клетках (Рис. 2Г).
Рис. 2. Сверхэкспрессия и аберрантная локализация TERC в иПСК WRS. (А) Анализ экспрессии TERC методом ОТ-кПЦР в контрольных и полученных от пациентов фибробластах и линиях иПСК (пассаж 7). Погрешности указывают на стандартную ошибку среднего (SEM), n=5 (* P < 0,05–0,01, ***P < 0,001, непарный t-критерий Стьюдента). (Б) FISH-анализ РНК TERC в сочетании с иммуноокрашиванием нуклеолином был проведен на контрольных и иПСК WRS. Показаны репрезентативные изображения фрагментов колоний иПСК. Масштаб: 20 мкМ. (В) Количественная оценка колокализации TERC с нуклеолином. На графиках представлены коэффициенты корреляции Пирсона (PCC) и Мандерса (MCC), где M1 представляет собой корреляцию сигналов РНК TERC с нуклеолином, а M2 – корреляцию нуклеолина с сигналами РНК TERC. Горизонтальная линия представляет собой медиану, границы ячеек соответствуют первому и третьему квартили, а усы ячеек охватывают диапазон данных от минимального до максимального. n>100, ***P<0,001, непарный t-критерий. (Г) FISH-анализ TERC РНК в сочетании с иммуноокрашиванием антителами к нуклеолину проводился на фибробластах контрольных и WRS. Показаны репрезентативные снимки ядер фибробластов. Масштаб: 20 мкМ (Orlova et al., 2025; разрешение предоставлено издательством Springer Nature, номер лицензии 6161991081406).
Также было установлено, что иПСК WRS демонстрируют более высокий уровень сигнала маркера двухцепочечных разрывов ДНК, гистона γH2AX, по сравнению с контрольными иПСК и иПСК HGPS. Часть сигналов γH2AX обнаружена в теломерах иПСК WRS. Анализ относительной длины теломер в иПСК по сравнению с исходными фибробластами показал отсутствие удлинения теломер при репрограммировании клеток WRS в отличие от контрольных. Полученные результаты свидетельствуют о нарушении стабильности теломер в стволовых клетках при синдроме Видемана-Раутенштрауха.
Данное исследование раскрывает фундаментальное различие в молекулярных механизмах развития прогероидного фенотипа при HGPS и WRS. Ключевое открытие — отсутствие обновления клеток при репрограммировании фибробластов с синдромом WRS, связанное с повышенной экспрессией мутантного POLR3A.
Нами впервые было показано, что мутации POLR3A связаны с аномалиями ядрышка и нарушением биогенеза теломеразной РНК в стволовых клетках WRS. Ядерная компартментализация компонентов теломеразы играет важную роль в сборке теломеразы. Задержка TERC в ядрышке, наблюдаемая в клетках WRS, может приводить к снижению эффективности работы теломеразы и, следовательно, влиять на удлинение теломер в стволовых клетках. Хотя ген POLR3A не относится к генам теломеразного комплекса, однако его мутации приводят к сходным симптомам, наблюдаемым при синдромах, вызванных мутациями генов теломеразы или теломерного защитного комплекса, что позволяет отнести синдром Видемана-Раутенштрауха к группе теломеропатий. Таким образом, линия иПСК из клеток пациентов с WRS может стать важной моделью для разработки новых подходов в лечении, направленного на предотвращение преждевременного старения стволовых клеток.
Новость подготовила
© Орлова Евгения Алексеевна, м.н.с. лаборатории эпигенетики развития ИБР РАН.
21.01.2026