22(1): 2. https://doi.org/10.1186/s12983-024-00554-y
© 2025 The Authors. Open Access. Published by BioMed Central. This is an open access article under the CC BY license
(Creative Commons Attribution 4.0 International License, http://creativecommons.org/licenses/by/4.0/)

Научные интересы: апиология.


Область научных интересов: генетика, молекулярная биология, энтомология, популяционная генетика.
Способность связывать запах с условиями пространства и времени обеспечивает фуражирующим насекомым важное эволюционное преимущество в поддержании жизнедеятельности семьи. Особенно развитые механизмы восприятия запахов сформировались у медоносных пчел (Apis mellifera). Они являются удобной моделью для изучения роли запах-связывающих белков (OBP) в обонятельном поведении, поскольку соединяют большое разнообразие поведенческих адаптаций с относительной простотой нейрональной архитектуры и умеренным по размеру геномом (Liu et al., 2025).
Обоняние определяет важные аспекты фуражировочного поведения социальных насекомых. В этом важную роль играют OBP — белки, выступающие посредниками между летучими молекулами и обонятельными нейронами (Liu et al., 2025). Они способны избирательно связывать летучие молекулы и доставлять их к рецепторам обонятельных нейронов. В обществе медоносных пчел внимание к отдельным генам, таким как AmelOBP4, дает возможность понять, как химическая коммуникация адаптируется к социальным функциям. Показано, что AmelOBP4 экспрессируется на более высоком уровне в антеннах и у пчел-нянек, и у фуражиров, что подчеркивает его универсальное участие в восприятии запахов независимо от возраста и кастовой специализации (Liu et al., 2025). Эти белки не ограничиваются ролью транспортеров: они способны модифицировать сенсорную чувствительность и влиять на сложные формы поведения, от выбора кормовых источников до реакции на феромоны расплода.
Обоняние включает несколько этапов, в процессе которых происходит захват молекул, преобразование химического сигнала в электрическую активность и формирование поведенческого ответа (Wilson & Mainen, 2006). OBP расположенны в лимфе сенсилл хеморецепторных органов (Pelosi et al., 2014), в которых они активируют специализированные нейроны (Pophof, 2002). Они доставляют летучие вещества к специфическим рецепторам (OR), инициируя поведенческие реакции (Fan et al., 2011; Leal, 2013). Мутации в OBP могут радикально менять поведение. Это подчеркивает многофункциональность OBP, которые оказываются не просто переносчиками, но частью сложной сенсорной системы.
Медоносная пчела Apis mellifera традиционно используется для исследования механизмов поведения, нейробиологии и молекулярной генетики (Mogily et al., 2020). Геном Apis mellifera содержит 21 ген OBP (Foret & Maleszka, 2006), преимущественно экспрессирующихся в сенсиллах антенн. Было установлено, что AmelOBP1 распознает феромон матки (Wu et al., 2022), AmelOBP2 и AmelOBP13 — разнообразные растительные летучие вещества (Briand et al., 2001; Iovinella et al., 2011), а AmelOBP14 — главным образом терпеноиды (Spinelli et al., 2012).
Экспрессия AmelOBP4 заметно выше в головах пчел-фуражиров, чем у пчел-нянек, независимо от возраста (Liu et al., 2019), что указывает на связь между экспрессией гена и разделением труда. В рамках рассматриваемого исследования был выполнен филогенетический анализ и охарактеризованы тканевые и возрастные профили экспрессии AmelOBP4 у пчел. Затем при помощи RNA-интерференции (RNAi) снижали уровень экспрессии AmelOBP4, оценивая изменения реакции на сахар и на панель запаховых стимулов. Эти подходы позволяют выявить консервативные механизмы сенсорной пластичности.
Таблица 1. Праймеры, использованные в этом исследовании для синтеза двухцепочечной РНК гена AmelOBP4 и количественной полимеразной цепной реакции с обратной транскрипцией (ОТ-кПЦР).
Подчеркнутые последовательности обозначают адаптер T7; F — прямой праймер; R — обратный праймер.
В экспериментах по функциональному нокдауну AmelOBP4 использовали два варианта двуцепочечной РНК: dsAmelOBP4 для снижения экспрессии гена и dsGFP в качестве негативного контроля.
Для поведенческих тестов использовали по 50 пчел-нянек и фуражиров из одной семьи пчел. Половина пчел получала dsAmelOBP4, остальные — dsGFP. Через 24 часа оценивали сахарную чувствительность при помощи рефлекса вытягивания хоботка (proboscis extension response, PER), который является классическим инструментом анализа сенсорной мотивации у медоносных пчел (Pankiw & Page, 1999). Это позволяет связывать молекулярные изменения, вызванные RNAi, с физиологическими и поведенческими показателями.
Для оценки обонятельной функции AmelOBP4 был использован расширенный набор химических стимулов. На основе исследований связывания OBP14 у Apis mellifera и у Apis cerana (Peng et al., 2021) сформировали панель из десяти растительных летучих соединений и четырех компонентов феромона расплода. Все вещества растворяли в n-гексане; n-гексан использовали в качестве контрольного стимула.
Дополнительно проводили поведенческий анализ в Y-образном ольфактометре (Gilmont Instr., Barnant Co., Barrington, IL, United States). Одну пчелу выпускали в центральный канал, фиксировали направление ее выбора и время достижения выбранной ветви. Отсутствие решения в течение более 5 минут считали нерешительностью и исключали из анализа. Для каждого вещества тестировали 45–60 пчел, происходящих из трех разных семей. Эти интегрированные поведенческие тесты — EAG и Y-образный ольфактометр — позволяют объективно оценивать, как нокдаун OBP изменяет обонятельную чувствительность и выбор запахов, показывая связь между уровнем гена и обонятельным поведением.
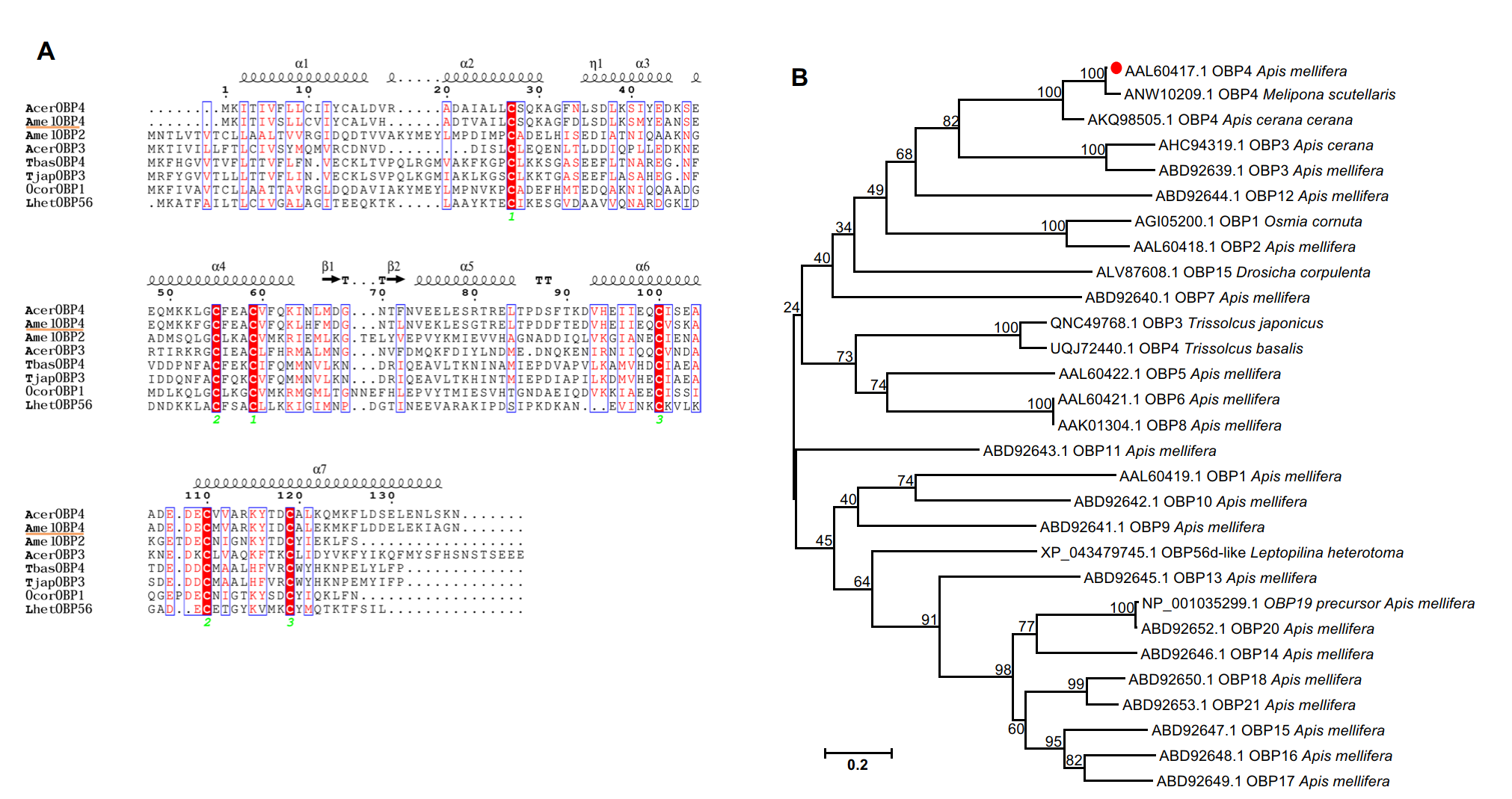
Было выявлено что AmelOBP4 содержит шесть консервативных цистеинов, формирующих три дисульфидные связи (Рис. 1A). Филогенетический анализ (Рис. 1B) показывает высокую степень родства с OBP4 других представителей Hymenoptera. Данные высокопроизводительного секвенирования выявили усиленную экспрессию AmelOBP4 в головах фуражиров.
Рис. 1. А. Сравнение аминокислотных последовательностей AmelOBP4 с OBP4 других видов. TbasOBP4: OBP4 Trissolcus basalis; OcorOBP1: OBP1 Osmia cornuta; LhetOBP56d: OBP56d Leptopilina heterotoma. Красным цветом выделены консервативные аминокислотные домены, в том числе шесть высококонсервативных цистеинов (обозначены зелеными цифрами ниже). Предсказанные вторичные структуры (например, ?-спираль) показаны над соответствующими последовательностями. B. Филогенетическое древо белков семейства AmelOBPs с другими гомологичными белками, основанное на методе Neighor-присоединения (Bootstrap = 1000 раз) с использованием программного обеспечения MEGA 6.0
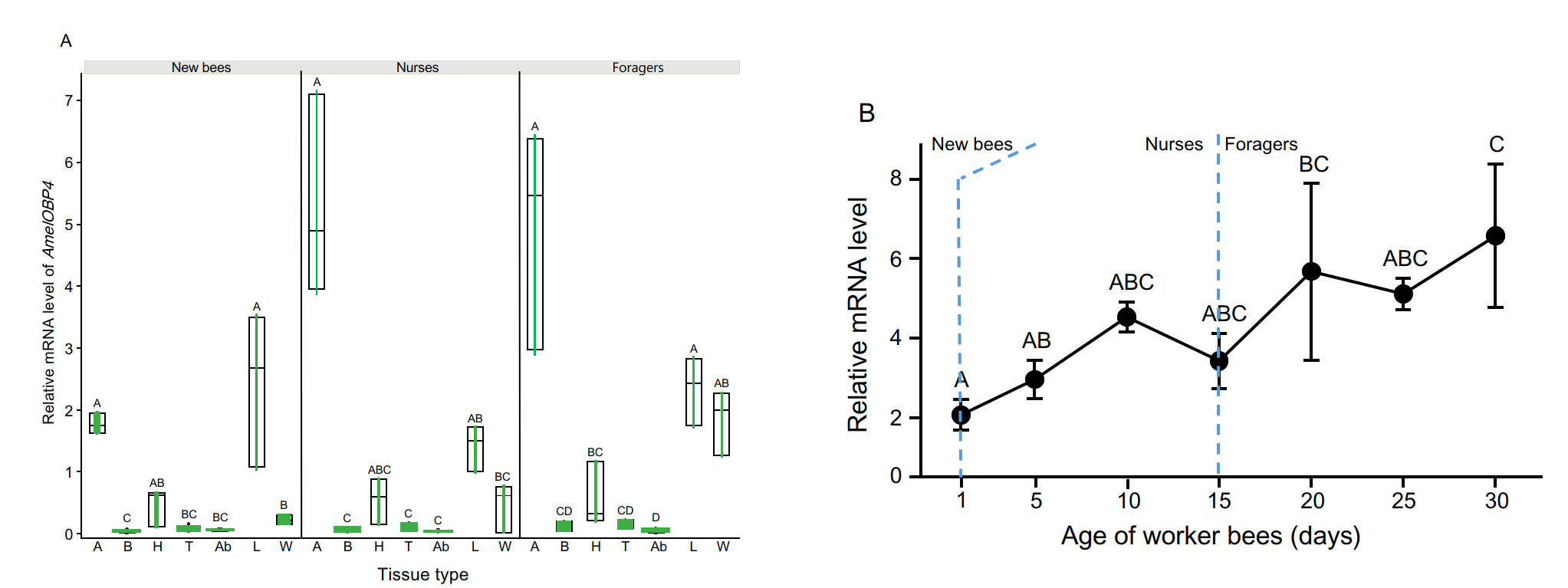
Рис. 2. А. Показан относительный уровень экспрессии AmelOBP4 в антеннах, головном мозге, грудной клетке, брюшке, ногах, крыле и голове (без мозга) у молодых пчел, пчел-нянек и фуражиров. B. Экспрессия AmelOBP4 в усиках рабочих пчел разного возраста (0–1: молодые пчелы; 5–15: пчелы-няньки; > 15: пчелы-фуражиры). Уровень мРНК AmelOBP4 анализировали с помощью REML-анализа с последующим тестом Тьюки для множественных сравнений (n = 3 для каждой точки). Разные буквы обозначают значимые различия. A: усики; B: мозг; H: голова; T: грудная клетка; Ab: брюшко; L: нога; W: крыло.
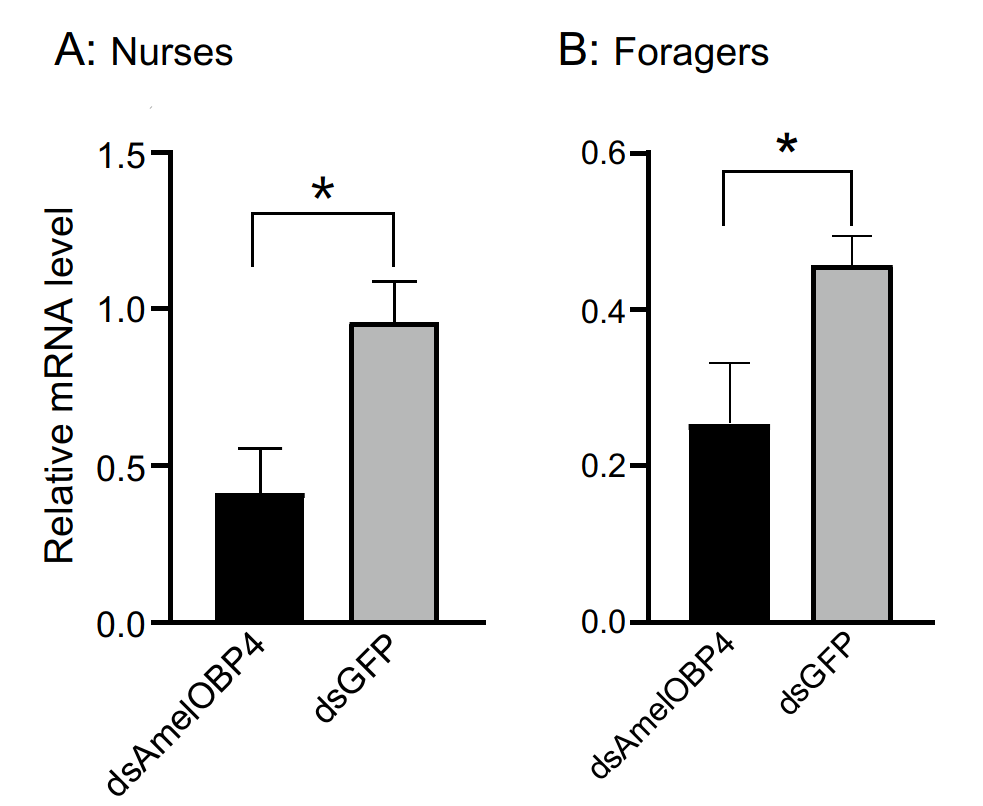
Для прямой оценки роли гена был проведен RNAi-нокдаун у нянек и фуражиров. Уровень экспрессии AmelOBP4 в антеннах достоверно снизился на 44,2% у пчел-нянек и на 57% у фуражиров (Рис. 3).
Рисунок.3. Уровень мРНК AmelOBP4 в антеннах пчел-нянек (A) и фуражиров (B) после кормления dsAmelOBP4 или dsGFP. Представлен результат независимого t-критерия, данные представлены в виде среднего значения ± стандартная ошибка (n = 3). * Указывает на значимую разницу при P < 0,05 по сравнению с контрольной группой.
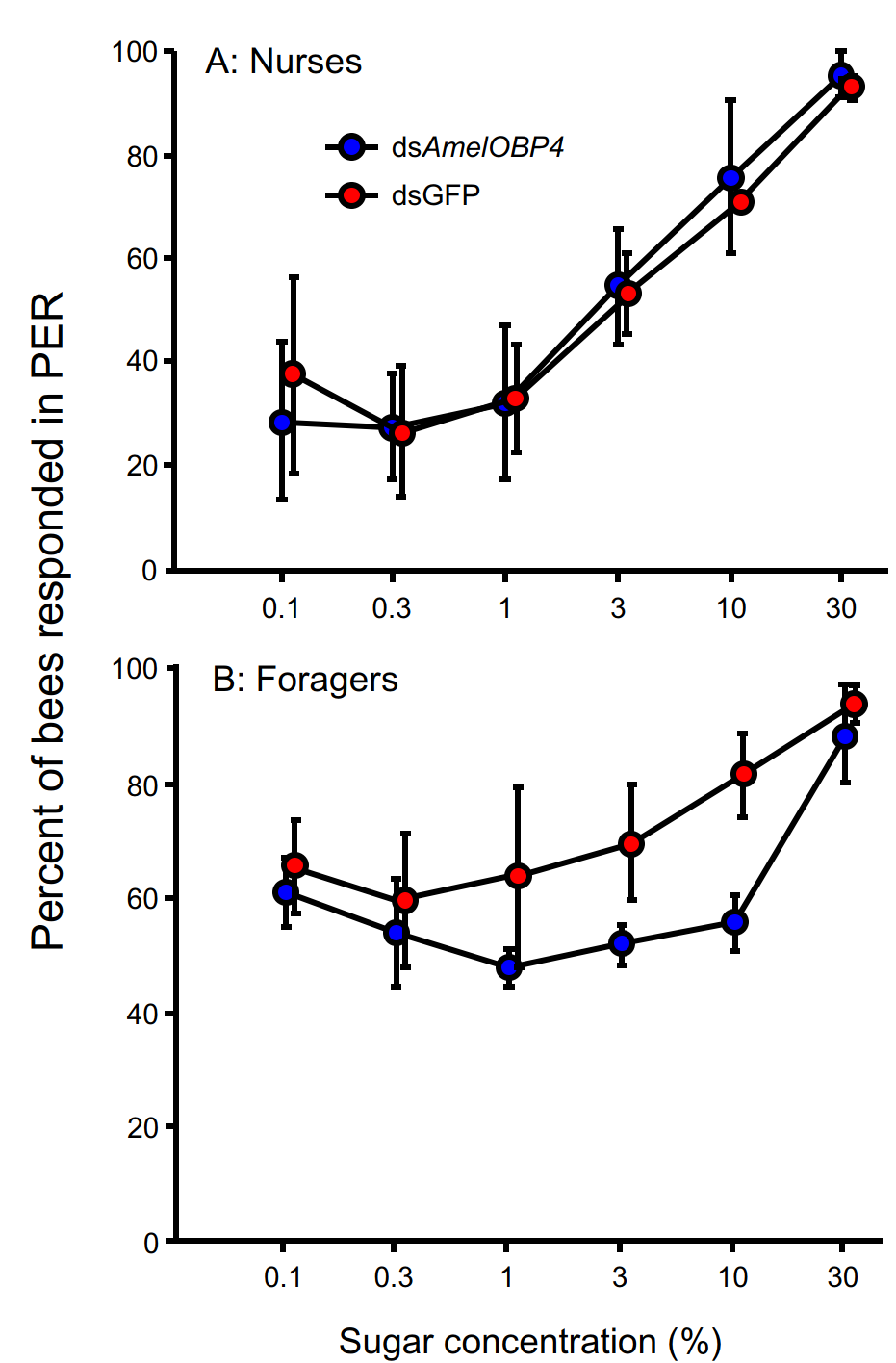
В тесте PER реакция фуражиров зависела от концентрации сахарозы. Нокдаун AmelOBP4 вызывал выраженное снижение вероятности ответа (Рис. 4B), при этом взаимодействие факторов оказалось статистически незначимым. Эти результаты выявляют, что снижение уровня AmelOBP4 нарушает нормальную сенсорную мотивацию.
Рисунок.4. Средняя оценка (% ± стандартная ошибка) реакции фуражиров (A) и пчел-нянек (B) на различные концентрации сахара после введения dsAmelOBP4 или dsGFP. Реакция на сахарозу была значительно (P < 0,01) снижена у фуражиров, получавших dsAmelOBP4, по сравнению с контрольной группой, получавшей dsGFP. Реакция на сахарозу у пчел-нянек, получавших dsAmelOBP4, не отличалась существенно (P > 0,05) от реакции пчел-нянек, получавших dsGFP. Данные по трем ульям были проанализированы после преобразования арсином в ходе дисперсионного анализа ANOVA, но представлены здесь без преобразования.
У пчел-нянек чувствительность к сахарозе закономерно изменялась в зависимости от концентрации раствора. Однако введение dsAmelOBP4 не вызывало значимых различий между экспериментальной и контрольной группами (Рис. 4A), и взаимодействие факторов также отсутствовало.
Электроантенография (EAG) после подавления экспрессии AmelOBP4 подтверждает эти поведенческие закономерности (Рис. 5).
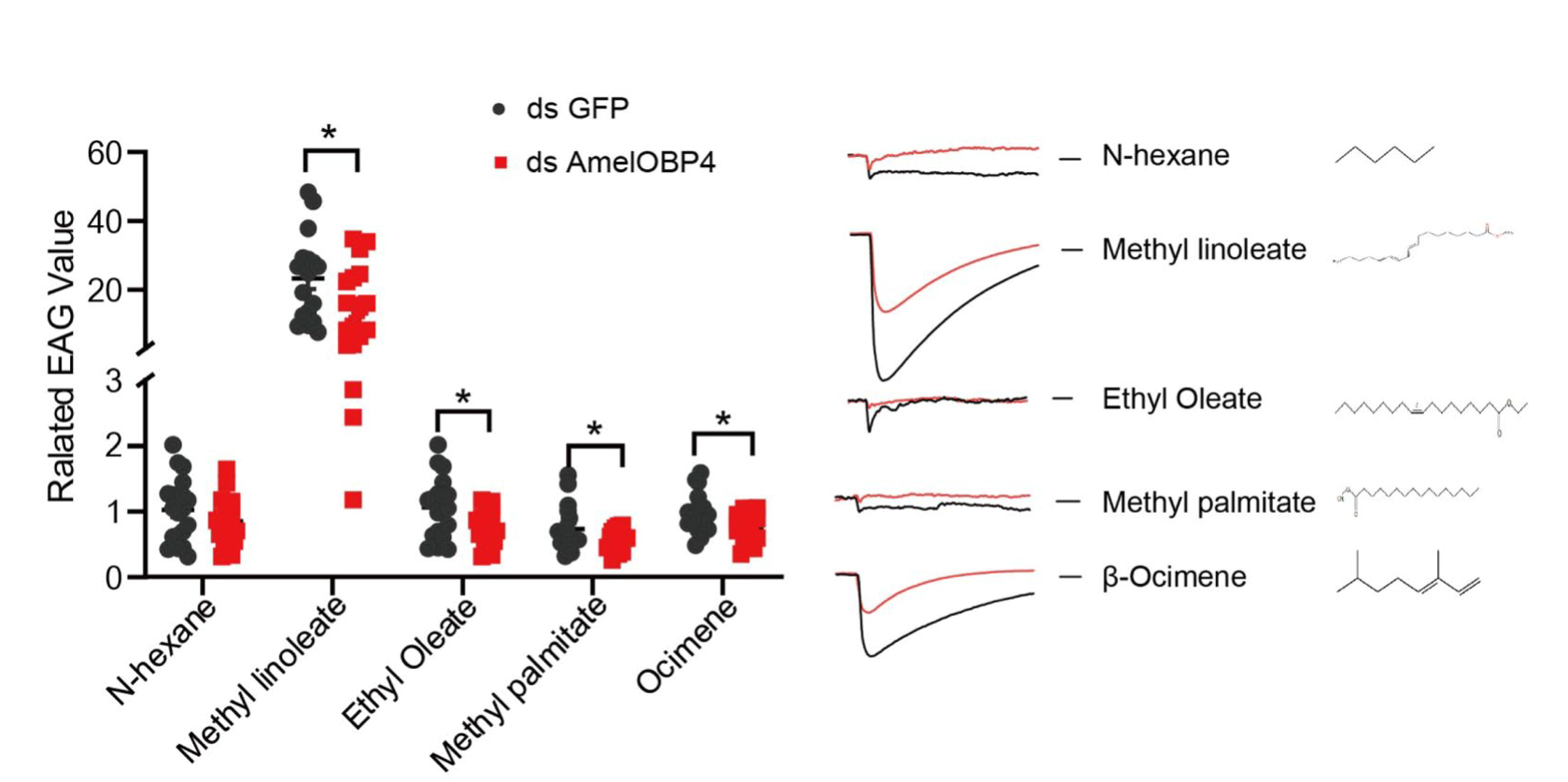
Рисунок.5. Реакция EAG пчел-нянек на феромон расплода метил линолеат, этил олеат, метил пальмитат и β-оксимен. Все данные представлены в виде среднего значения ± стандартная ошибка (n = 15). Звездочки обозначают значимую разницу, выявленную с помощью дисперсионного анализа (*p < 0,05)
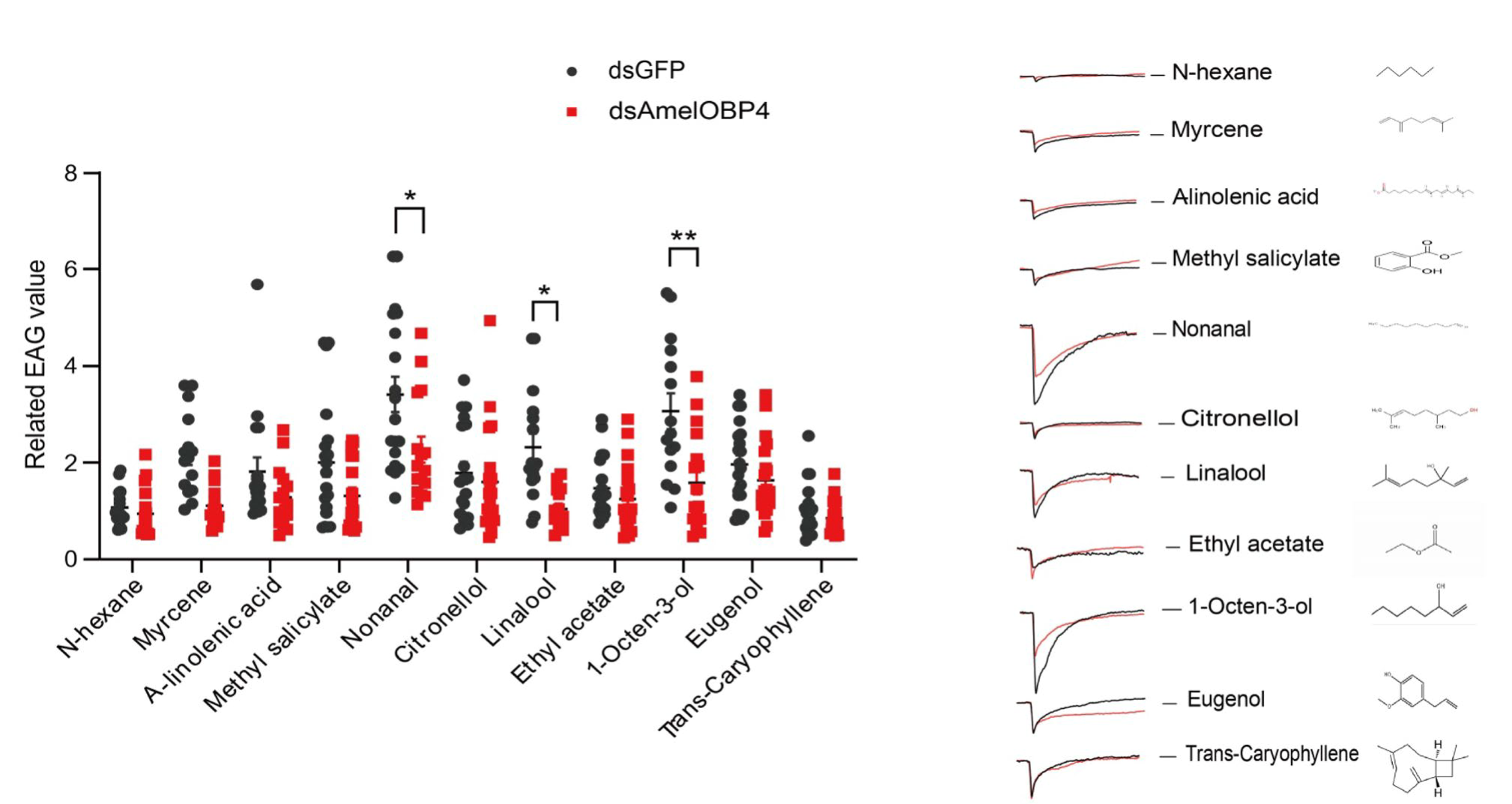
У фуражиров эффекты RNAi были более избирательными (Рис. 6). Такая разница в спектре воспринимаемых веществ подчеркивает, что сенсорная роль AmelOBP4 функционально варьирует между поведенческими кастами.
Рисунок 6. Реакция EAG фуражиров на летучие вещества растений: н-гексан, мирцен, ?-линденевую кислоту, метилсалицилат, нонаналь, цитронеллол, линалоол, этилацетат, 1-октен-3-ол, эвгенол и транс-кариофиллен. Все данные представлены в виде среднего значения ± стандартная ошибка (n = 15). Звездочки обозначают статистически значимую разницу, установленную с помощью дисперсионного анализа (*p < 0,05; **p < 0,01).
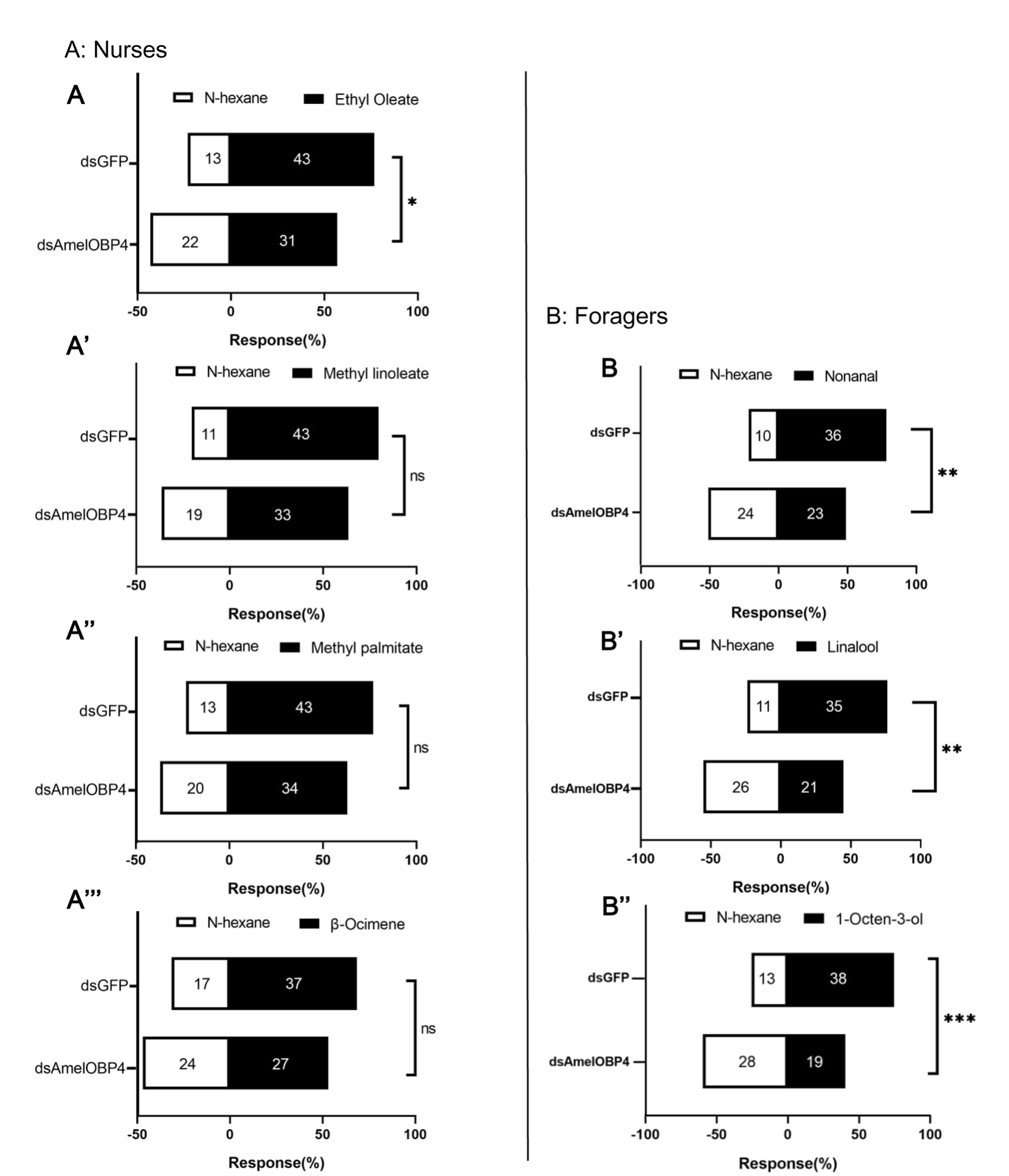
Анализ выбора в Y-образном ольфактометре показывает, что снижение экспрессии AmelOBP4 приводит к специфичным изменениям в обонятельных предпочтениях (Рис. 7A). У фуражиров подавление AmelOBP4 приводило к существенному снижению привлекательности летучих сигналов цветочного происхождения.
Рис. 7. Количественная оценка обонятельных реакций пчел-нянек на компоненты феромонов расплода: этилолеат (A), метиллинолеат (A’), метилпальмитат (A’’) и β-оцимен (A’’’), а также обонятельных реакций фуражиров на летучие вещества растений: нонаналь (B), линалоол (B’) и 1-октен-3-ол (B’’). Статистический анализ проводился с использованием критерия хи-квадрат. **: p < 0,001; *: p < 0,05, нс: p > 0,05
Эти наблюдения указывают, что AmelOBP4 играет дифференцированную и поведенчески значимую роль в обеспечении обонятельной чувствительности рабочих пчел.
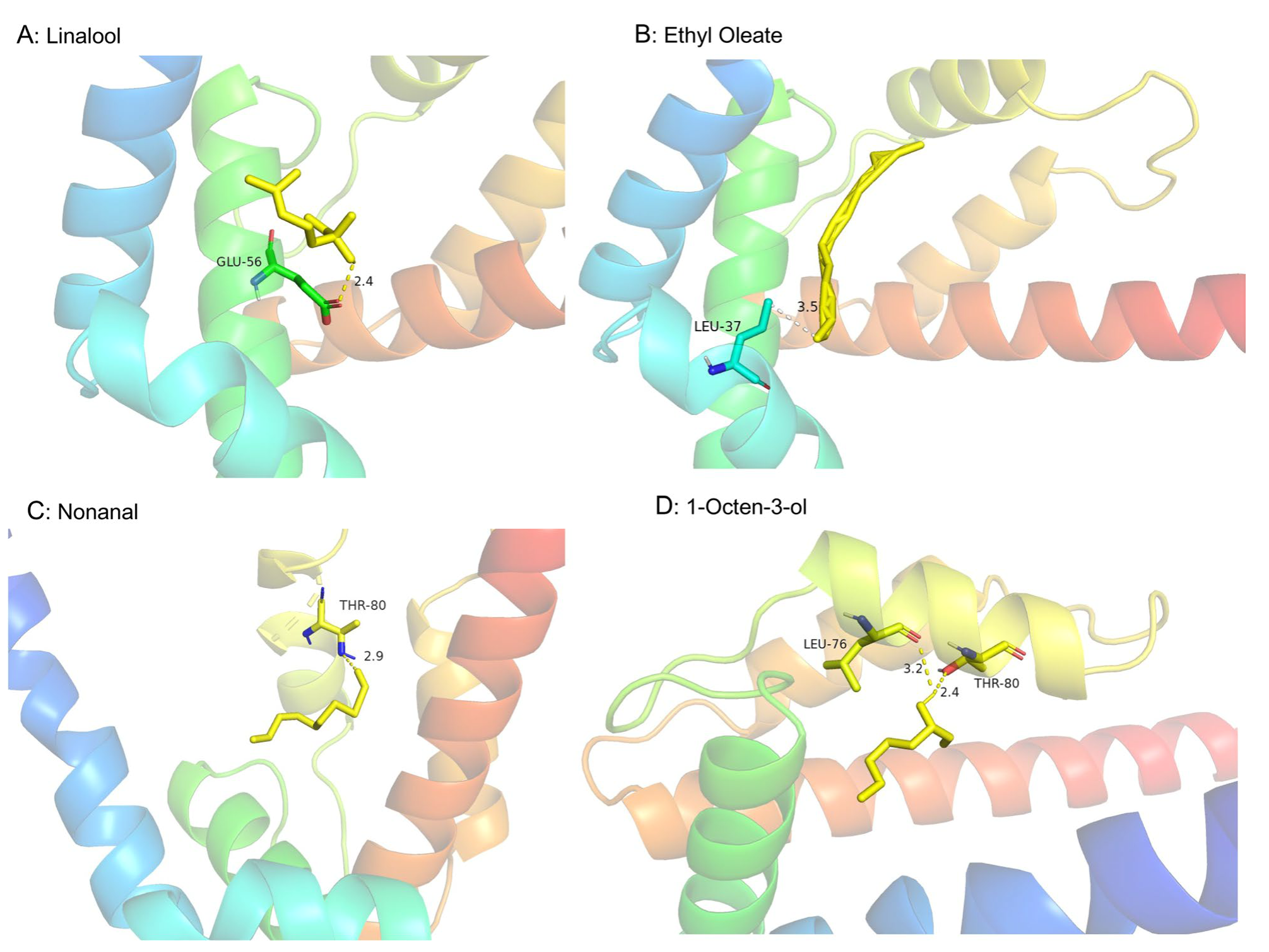
Структурная организация AmelOBP4 была предсказана на основе гомологичного белка AcerOBP4, с которым он имеет высокое аминокислотное сходство — 78,68% (Рис. 8.)
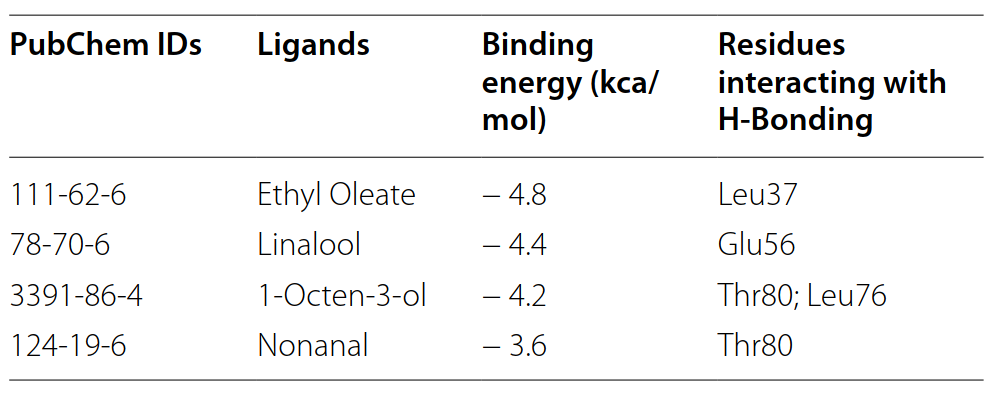
Рисунок 8. Водородные связи, образованные между этилолеатом, линалоолом, нонаналом, 1-октен-3-олом и AmelOBP4, согласно прогнозу программы Auto dock. Субстраты этилолеат, линалоол, нонанал и 1-октен-3-ол показаны голубым цветом, потенциальные водородные связи обозначены пунктирными линиями синего цвета, лиганды показаны желтым цветом
Представленные результаты органично вписываются в общий контекст исследований OBP у насекомых. В случае медоносной пчелы особенно примечателен факт, что уровни экспрессии AmelOBP4 остаются повышенными как в антеннах, так и в ногах у нянек и фуражиров. Такой распределенный паттерн предполагает участие белка не только в обнаружении экологически значимых летучих веществ, но и в обработке запахов, связанных с внутренними социальными сигналами (Pankiw, 2004; Scheiner et al., 2004).
Аналогично тому, что было показано для AcerOBP4 у Apis cerana (Li et al., 2023), экспрессия AmelOBP4 у Apis mellifera отображает возраст-зависимый рост и сохраняет стабильные уровни при переходе рабочей пчелы от роли няньки к роли фуражира.
У пчел-нянек экспрессия AmelOBP4 также остается высокой, однако нокдаун не приводит к изменению сахарной отзывчивости.
Снижение поведенческой предпочтительности у медоносных пчел — как у нянек, так и у фуражиров — после подавления AmelOBP4 демонстрирует общую закономерность: вмешательство в работу OBP напрямую влияет на способность насекомых различать и оценивать ключевые стимулы.
Интересно, что у нянек снижение амплитуды EAG-ответа на β-оцимен не сопровождается изменением их поведенческого выбора (Рис. 7A). Такой результат отражает особую биологическую роль β-оцимена (Traynor et al., 2015), а также служит индикатором наличия расплода (Maisonnasse et al., 2010).
Данные молекулярного связывания предоставляют дополнительные структурно-функциональные аргументы. Подобно тому, как показано в исследованиях Pelosi et al. (2014), Lu et al. (2015) и Zhu et al. (2016), связывание лиганда с OBP определяется четкими контактными зонами.
Таблица 2. Параметры связывания этиллинолената, этилпальмитата, метиллинолеата, этилолеата, метилпальмитата и аминокислот AmelOBP4
В исследовании показано, что AmelOBP4 экспрессируется преимущественно в антеннах как пчел-нянек, так и фуражиров. Введение dsAmelOBP4 эффективно снижает экспрессию гена и приводит к уменьшению чувствительности к сахарам у пчел-фуражиров, тогда как у нянек PER остается практически неизменной. Тем не менее у нянек с нокдаун наблюдается снижение амплитуды EAG-ответа на феромоны расплода, тогда как у фуражиров EAG снижен на летучие соединения растений. Поведенческие тесты показывают, что подавление AmelOBP4 ослабляет обонятельные реакции и подтверждает функциональную значимость этого белка в восприятии основных химических сигналов.
У медоносной пчелы Apis mellifera выявлено 21 OBP, вовлеченных в регуляцию социальной жизни и коммуникации (Foret & Maleszka, 2006). Поведенческие эффекты нокдауна демонстрируют, что AmelOBP4 выполняет не только транспортную функцию, но и модулирует пороги чувствительности, интегрируя вкусовые и обонятельные сигналы (Swarup et al., 2014). У нянек снижение EAG на феромоны расплода может нарушать уход за потомством (Pankiw, 2004), тогда как у фуражиров уменьшение предпочтения летучих веществ растений может снижать эффективность сбора нектара.
Дополнительно, интеграция с циркадными ритмами предполагает, что экспрессия AmelOBP4 может модулироваться суточными циклами (Bloch et al., 2017)
В условиях антропогенного давления нарушение функций OBP может способствовать коллапсу пчелиных семей. Таким образом, AmelOBP4 является важнейшим компонентом для понимания эволюции обонятельной системы, регуляции поведения и сохранения биоразнообразия, а также имеет практическое значение для пчеловодства и экологии опылителей.
Список литературы
Briand L, Nespoulous C, Huet JC, Takahashi M, Pernollet JC: Ligand binding and physico-chemical properties of ASP2, a recombinant odorant-binding protein from honeybee (Apis mellifera L.). Eur J Biochem 2001, 268:752–60.Fan J, Francis F, Liu Y, Chen JL, Cheng DF: An overview of odorant-binding protein functions in insect peripheral olfactory reception. Genet Mol Res 2011, 10:3056–69.
Foret S, Maleszka R: Function and evolution of a gene family encoding odorant binding-like proteins in a social insect, the honey bee (Apis mellifera). Genome Res 2006, 16:1404–13.
Iovinella I, Dani FR, Niccolini A, Sagona S, Michelucci E, Gazzano A, Turillazzi S, Felicioli A, Pelosi P: Differential expression of odorant-binding proteins in the mandibular glands of the honey bee according to caste and age. J Proteome Res 2011, 10:3439–49.
Leal WS: Odorant reception in insects: roles of receptors, binding proteins, and degrading enzymes. Annu Rev Entomol 2013, 58:373–91.
Li Q, Liu F, Zhao HX, Zhao JX: Molecular characterization and spatiotemporal expression of odorant binding protein gene OBP4 of Apis cerana. J Environ Entomol 2023, 45:488–93. (in Chinese).
Liu F, Shi T, Qi L, Su X, Wang D, Dong J, Huang ZY: lncRNA profile of Apis mellifera and its possible role in behavioural transition from nurses to foragers. BMC Genomics 2019, 20:393.
Liu F., Lai Y., Wu L., Li Q., Lei L., Yin W., Zhang Y., Huang Z. Y., & Zhao H. AmelOBP4: an antenna-specific odor-binding protein gene required for olfactory behavior in the honey bee (Apis mellifera). Frontiers in Zoology, 2025; 22(1): 2. https://doi.org/10.1186/s12983-024-00554-y
Lu Y, Yao Y, Zhang Q, Zhang D, Zhuang S, Li H, Liu Q: Olfactory biosensor for insect semiochemicals analysis by impedance sensing of odorant-binding proteins on interdigitated electrodes. Biosens Bioelectron 2015, 67:662–9.
Maisonnasse A, Lenoir JC, Beslay D, Crauser D, Le Conte Y: E-?-ocimene, a volatile brood pheromone involved in social regulation in the honey bee colony (Apis mellifera). PLoS ONE 2010, 5:e13531.
Mogily S, Vijaykumar M, Sethy SK, Joseph J: Characterization of the olfactory system of the giant honey bee, Apis dorsata. Cell Tissue Res 2020, 379:131–45.
Pankiw T, Page RE Jr: The effect of genotype, age, sex, and caste on response thresholds to sucrose and foraging behavior of honey bees (Apis mellifera L.). J Comp Physiol A 1999, 185:207–13.
Pankiw T: Brood pheromone regulates foraging activity of honey bees (Hymenoptera: Apidae). J Econ Entomol 2004, 97:748–51.
Pelosi P, Iovinella I, Felicioli A, Dani FR: Soluble proteins of chemical communication: an overview across arthropods. Front Physiol 2014, 5:320.
Peng Z, Huang L, Zhao SG, Lv JH, Zhao HT: Expression and ligand binding characterization of the odorant binding protein AcerOBP14 of Apis cerana cerana. Acta Entomol Sin 2021, 64:178–86. (in Chinese).
Pophof B: Moth pheromone binding proteins contribute to the excitation of olfactory receptor cells. Naturwissenschaften 2002, 89:515–8.
Scheiner R, Page RE, Erber J: Sucrose responsiveness and behavioral plasticity in honey bees (Apis mellifera). Apidologie 2004, 35:133–42.
Scheiner R: Responsiveness to sucrose and habituation of the proboscis extension response in honey bees. J Comp Physiol A 2004, 190:727–33.
Spinelli S, Lagarde A, Iovinella I, Legrand P, Tegoni M, Pelosi P, Cambillau C: Crystal structure of Apis mellifera OBP14, a C-minus odorant-binding protein, and its complexes with odorant molecules. Insect Biochem Mol Biol 2012, 42:41–50.
Swarup S, Morozova TV, Sridhar S, Nokes M, Anholt RR: Modulation of feeding behavior by odorant-binding proteins in Drosophila melanogaster. Chem Senses 2014, 39:125–32.
Traynor KS, Le Conte Y, Page RE: Age matters: pheromone profiles of larvae differentially influence foraging behaviour in the honeybee, Apis mellifera. Anim Behav 2015, 99:1–8.
Wilson RI, Mainen ZF: Early events in olfactory processing. Annu Rev Neurosci 2006, 29:163–201.
Wu F, Liu S, Zhang X, Hu H, Wei Q, Han B, Li H: Differences in ASP1 expression and binding dynamics to queen mandibular pheromone HOB between Apis mellifera and Apis cerana workers reveal olfactory adaptation to colony organization. Int J Biol Macromol 2022, 217:583–91.
Zhu J, Ban L, Song L-M, Liu Y, Pelosi P, Wang G: General odorant-binding proteins and sex pheromone guide larvae of Plutella xylostella to better food. Insect Biochem Mol Biol 2016, 72:10–9.
Новость подготовили
© д-р биол. наук Ильясов Рустем Абузарович
инженер-исследователь Ильясова Алла Юрьевна
старший лаборант Прокудина Софья Сергеевна
20.02.2026