Parasites & Vectors 2025, 18 (1), 28. doi: 10,1186/s13071-025-06673-7

Научные интересы: апиология.

Эктопаразитический клещ Varroa destructor оказывает негативное влияние на популяции медоносной пчелы Apis mellifera и служит фактором снижения числа семей и приводит к большим экономическим потерям в пчеловодстве (Rosenkranz et al., 2010). В отличие от своего первоначального хозяина восковой пчелы Apis cerana, где паразитизм ограничен только трутневым расплодом, в гнезде медоносной пчелы A. mellifera клещ V. destructor поражает весь расплод, что приводит к более высокому уровню зараженности (Rosenkranz et al., 2010). Клещ питаетcя тканями взрослых особей и гемолимфой преимагинальных стадий, вызывая множественные патофизиологические эффекты: снижение массы при выходе, дефицит сперматогенеза у трутней, нарушение полетов и навигации и подавление иммунитета у пчел (Noël et al., 2020; Di Prisco et al., 2016). Кроме того, клещ Varroa служит резервуаром и переносчиком вирусов, в частности вируса деформации крыльев Deformed wing virus (DWV), что в стрессовых условиях может приводить к гибели всей семьи пчел (Di Prisco et al., 2013; Di Prisco et al., 2016). Сочетание клеща Varroa с другими биотическими и абиотическими стрессорами (пестициды, патогены, климат) усиливает его негативное влияние на семьи пчел (Straub et al., 2019; Morfín et al., 2023). При отсутствии лечения семьи пчел зачастую погибают от клеща в интервале от 1 до 3 лет (Fries et al., 2006).
Традиционные методы борьбы с клещом включают химические акарициды (формамидины, органофосфаты, пиретроиды), которые дают быстрый эффект, но приводят к накоплению химических остатков в продуктах пчеловодства, неблагоприятному влиянию на здоровье пчел и развитию резистентности у клещей (González-Cabrera et al., 2018; Hernández-Rodríguez et al., 2021; Bajuk et al., 2017). В связи с экологическими целями и политикой по сокращению использования химических пестицидов (European Green Deal), возрастающая потребность в альтернативных, целевых и экологичных методах борьбы с вредителями становится приоритетом (Fletcher et al., 2020). RNA-интерференция (RNAi) рассматривается как перспективный инструмент, обеспечивающий селективное подавление экспрессии генов-мишеней у клещей Varroa посредством целевой двухцепочечной РНК (dsRNA), что делает этот подход потенциальной альтернативой применению химических акарицидов (Wilson & Doudna, 2013; Parker et al., 2019).
Существуют ранее опубликованные лабораторные эксперименты эффективности RNAi против различных патогенов пчел и паразитов: снижение нагрузки вируса DWV при приеме dsRNA (Desai et al., 2012), подавление вируса израильского острого паралича IAPV (Maori et al., 2009; Hunter et al., 2010), контроль размножения вируса мешотчатого расплода SBV (Liu et al., 2010; Yoo et al., 2023), воздействие на микроспоридию Vairimorpha ceranae (Paldi et al., 2010; Huang et al., 2016) и подавление развития ульевого жука Aethina tumida (Powell et al., 2017). Ранее были показаны лабораторные результаты РНК-интерференции клещей Varroa посредством инъекций в них dsRNA или замачивания их в воде с dsRNA или кормления пчел сахарным сиропом с dsRNA, что приводило к снижению выживаемости и фертильности клещей (Campbell et al., 2010; Garbian et al., 2012; McGruddy et al., 2024; Leonard et al., 2020). Однако до настоящего времени отсутствуют надежные доказательства эффективности RNAi в реальных условиях пасеки.
Цель исследования заключалась в оценке эффективности и применимости схемы перорального введения смеси dsRNA, нацеленной на функционально значимые гены V. destructor, в условиях естественного пчеловодства (Bortolin et al., 2025). В качестве мишеней для RNAi выбраны гены, связанные с мишенями известных акарицидов: ацетил-CoA-карбоксилаза (VdACC), Na+/K+-ATPase (VdATPase) и эндохитиназа (VdChit). VdACC участвует в липидном метаболизме и является мишенью акарицидов семейства тетроновых/тетрамических кислот (Lümmen et al., 2014); VdATPase регулирует ионный баланс и может быть поражена растительными токсинами (Ding et al., 2020; Shang et al., 2021); VdChit участвует в деградации и реконструкции хитина при линьке, и угнетение его экспрессии нарушает развитие клеща (Zhou et al., 2017). Были разработаны короткие фрагменты dsRNA (VdACC-dsRNA 248 п.н.; VdATPase-dsRNA 249 п.н.; VdChit-dsRNA 211 п.н.) по последовательностям V. destructor с предварительной проверкой на отсутствие значимых нецелевых совпадений в геноме A. mellifera. В качестве отрицательного контроля использовался dsRNA зеленого флуоресцентного белка GFP (432 п.н.) (Desai et al., 2012; Maori et al., 2009). Синтез dsRNA был выполнен in vitro коммерческой компанией AgroRNA, с хранением при −20 °C до применения (Bortolin et al., 2025).
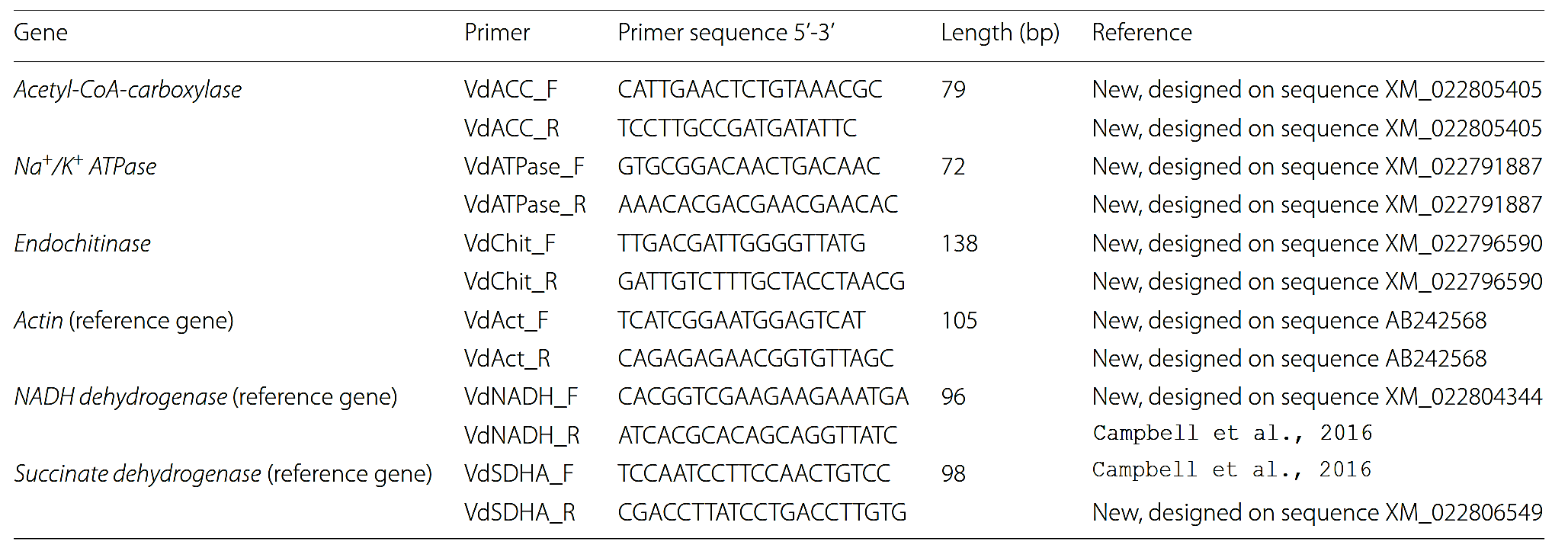
Для валидации способности dsRNA к RNAi у V. destructor были проведены эксперименты замачивания клещей в водных растворах dsRNA (2,5 μg/μl) и последующий отбор выживших клещей для анализа qPCR экспрессии через 48 ч. со специально разработанными праймерами (Табл. 1).
Таблица 1. Праймеры использованные в данном исследовании для количественной ПЦР
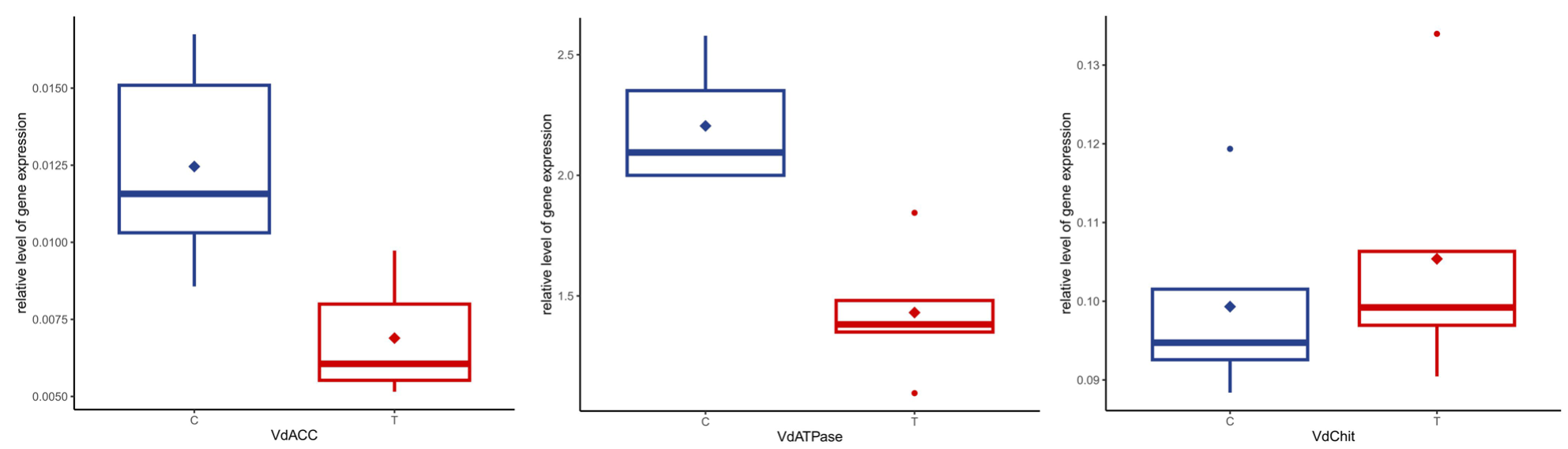
Итогом стало существенное снижение уровней транскриптов ACC и Na+/K+-ATPase (в среднем на 45% и 35% соответственно; t-тесты, P = 0,0064 и P = 0,0008), тогда как для эндохитиназы значимого снижения отмечено не было (Рис. 1) (Bortolin et al., 2025). Для нормализации qPCR использовался генный набор, проверялись Actin, NADH dehydrogenase (NADH) и succinate dehydrogenase (SDHA), из которых SDHA был признан наиболее подходящим референсным геном по стабильности и сопоставимости Ct (Campbell et al., 2016).
Рисунок 1. Относительные уровни экспрессии генов ацетил-CoA-карбоксилазы Varroa destructor (VdACC), Na+/K+-ATPase V. destructor (VdATPase) и эндохитиназы V. destructor (VdChit), нормированные на уровень экспрессии гена SDHA, в контрольной (C) и опытной (T) группах. На графике прямоугольники показывают межквартильный размах, с медианой (поперечная линия) и средним значением (ромбы); вертикальные линии — вариационные размахи за исключением выбросов (точки). Для гена VdChit различия ни по среднему, ни по медианным значениям статистически не значимы.
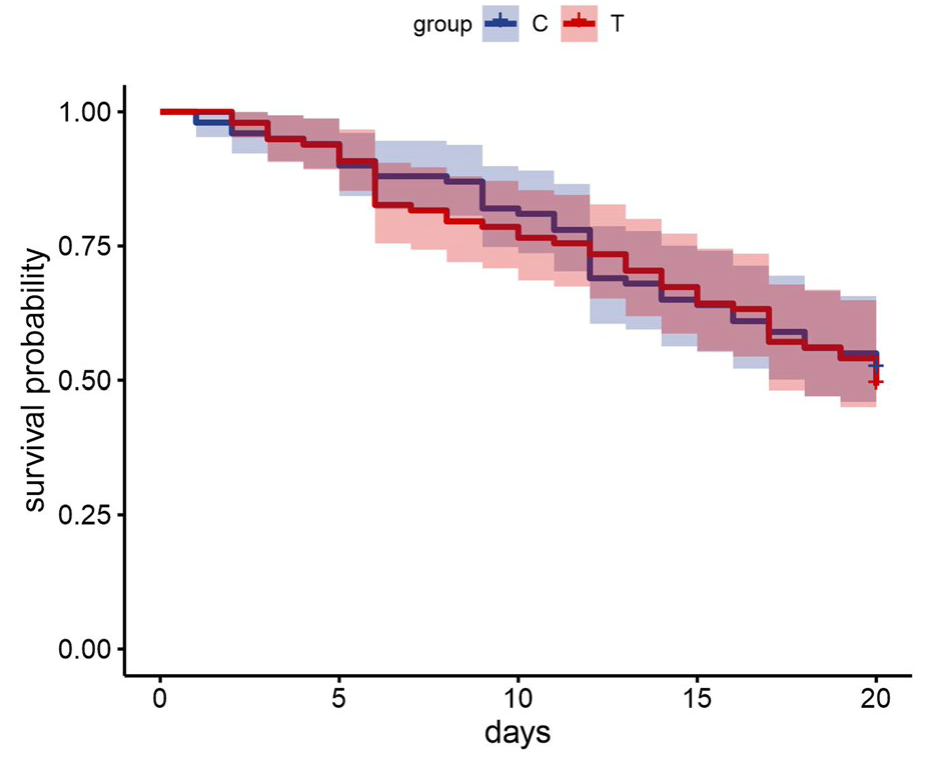
Пероральное введение смеси dsRNA (по 1 μg каждого dsRNA на пчелу в день первые 7 дней) в мини-ульях (31–35 пчел) не оказало статистически значимого влияния на выживаемость по сравнению с контролем (χ ² = 0,11, P = 0,73) (Рис. 2) (Bortolin et al., 2025). Дополнительная полевого наблюдения за силой семей пчел (расплод и взрослые особи) также не выявила значимых различий между группами в конце эксперимента (ANOVA, P > 0,3). Эти данные согласуются с предыдущими работами, отмечающими общую нечувствительность взрослых медоносных пчел к dsRNA (Tan et al., 2016; Hollowell & Rieske, 2022; Chen et al., 2015).
Рисунок 2. Кривые выживаемости Каплана-Мейера для пчел, которых кормили смесью dsRNA (T), в сравнении с пчелами, которых кормили только сахарозным раствором (C). Затененные области представляют 95% доверительные интервалы.
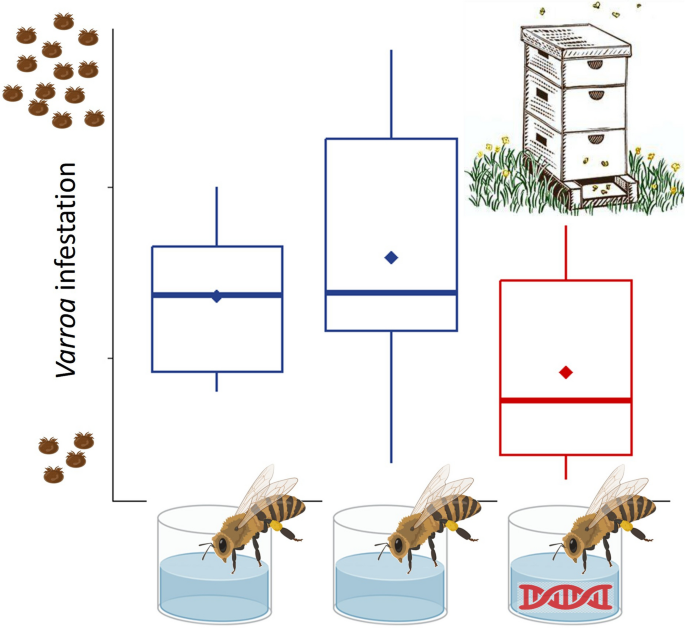
Полевой этап эксперимента проводился на 50 семьях в 5 пасеках региона Veneto (Италия) с отбором по одинаковой силе семей в ульях Дадана-Блатта, 10 рамок. Оценка силы семей пчел и контроль болезней проводились в 1, 16 и 37 день; оценивались также запасы меда и пыльцы по методу Liebefeld (Imdorf et al., 1987; Delaplane et al., 2013). Эксперимент проводился в 2022 году с 20 сентября по 9 ноября, с распределением на три группы: dsRNA mix (dsT) — 0,8 μg каждого dsRNA на пчелу/день, GFP контроль (gfpC) — 1 μg GFP-dsRNA на пчелу/день, и сахарозный контроль (sucC). Сироп подавался в виде 200 ml 60% сахарозы в вакуумных кормушках семь раз (раз в 3 дня). Уровень форетичного заражения определялся методом посыпки сахарной пудрой на ~300 взрослых пчел с трех реплик для каждой семьи, и вычислялся пост/пре коэффициент изменения заражения (IRpost/pre) между днем 1 и днем 37 (Macedo et al., 2002; Lee et al., 2010). Эксперимент был адаптирован к потребностям пчеловодов и не допускал инвазивных измерений внутри ячеек, чтобы не нарушать функционирование пчелиной семьи (Рис. 3) (Bortolin et al., 2025).
Рисунок 3. Экспериментальная оценка возможности и эффективности применения технологии РНК-интерференции для снижения численности клещей Varroa в естественных условиях содержания.
Из 50 исходных семей в окончательный анализ вошли данные 37 гнезд: 2 семьи исключены из-за их разорения (воровство и гибель матки), 10 семей погибли вследствие обработки комаров инсектицидами вблизи ульев, а еще одна — как аномалия с необычным динамическим снижением нагрузки клещом Varroa, не объясненным доступной информацией (Bortolin et al., 2025). Такой отбор обусловлен прагматическими ограничениями полевого эксперимента и переменной природной среды; авторы отмечают, что полевое проведение эксперимента в производственных ульях налагает ограничения на размер выборки и силу вмешательств.
Основным результатом стало то, что средний коэффициент изменения форетичной инфестации (IRpost/pre) в группе dsT оказался статистически значимо ниже, чем в группе GFP-контроля на 42% (t = 2,60, P = 0,0077) и чем в сахарозном контроле на 33% (t = 2,05, P = 0,0255). Медианный IRpost/pre также показал снижение на 45–46% относительно контролей (U тест Mann-Whitney, P ≈ 0,02–0,03) (Bortolin et al., 2025). Эти данные указывают на то, что пероральное введение смеси dsRNA, доставленное через кормление пчел, способно замедлить увеличение нагрузки клеща Varroa в семьях пчел в течение осеннего периода.
Механизм действия основан на способности dsRNA, принятой перорально взрослыми пчелами, распространяться гетерологично: горизонтальная передача через трофаллаксис и передача через маточное молочко между поколениями, что обеспечивает доступ dsRNA к клещам, питающимся гемолимфой расплода (Maori et al., 2019; Garbian et al., 2012). После всасывания dsRNA пчелами и передачи клещам возможно индуцирование RNAi в клещах и нарушение физиологии, что приводит к снижению выживаемости или фертильности (Garbian et al., 2012; Leonard et al., 2020). Разработанные меры по сохранению стабильности dsRNA (хранение при низкой температуре, чистота растворов, контроль потребления сиропа, теплоизоляция ульев) оказались важными для успеха полевого применения (Bortolin et al., 2025).
Авторы отмечают ряд ограничений в связи с невозможностью измерять динамику репродуктивной фазы клеща внутри расплода вследствие неприкосновенности продуктивных семей, а также в связи с ограниченным размером выборки из-за исключений и ограничений по вмешательству на пасеках. Также эффективность RNAi в целом сильно зависит от выбора мишеней, стадии развития паразита и молекулярных механизмов регуляции генов: в лабораторных экспериментах с замачиванием клещей три мишени показали разную чувствительность к РНК интерференции — гены VdACC и VdATPase успешно подавлялись, тогда как ген VdChit не показывал значимого снижения экспрессии, возможно, из-за регуляции на посттранскрипционном уровне или фазоспецифической экспрессии (Zhu & Palli, 2020; Belles, 2010; Chen et al., 2021). Потому предлагается подход подавлять экспрессию нескольких генов одновременно и нацеливание на разные участки одного гена для снижения риска формирования резистентности и повышения надежности эффекта.
В контексте практической применимости RNAi представляется многообещающей альтернативой химическим акарицидам, поскольку обеспечивает более селективное воздействие, меньшую персистентность в среде и потенциально более низкий риск для человека и животных (Parker et al., 2019; Schiemann et al., 2019). Отмечается, что European Food Safety Authority (EFSA) провел оценку рисков и классифицировал RNA-биопестициды как имеющие низкий риск при распылении для животных и людей, и что даже при возможном присутствии dsRNA в продуктах пчеловодства риск для человека мал благодаря барьеру кишечника и отсутствия совпадения последовательностей dsRNA с генами человека (Christiaens et al., 2018; Kleter, 2020). Эмпирические данные об остатках dsRNA в продуктах пчеловодства отсутствуют и требуют дальнейшего изучения (Bortolin et al., 2025).
В умеренном климате осенние обработки пчел от клеща Varroa важны для формирования зимующих популяций долгоживущих рабочих особей; воздействие на паразитов до формирования зимних пчел может повысить шансы успешной зимовки (Amdam et al., 2004). RNAi-подход в предлагаемом формате не устраняет клещей полностью, но способен удерживать осеннюю зараженность ниже порогов риска зимних потерь (Genersch et al., 2010). Однако для повышения эффективности следует определить оптимальные дозы dsRNA, частоту, длительность и время введения, а также возможную интеграцию с другими биотехнологическими методами контроля (Mancuso et al., 2020).
Список литературы
- Amdam G.V., Hartfelder K., Norberg K., Hagen A., Omholt S.W. Altered physiology in worker honeybees infested with Varroa destructor: a factor in colony loss during overwintering? Journal of Economic Entomology. 2004;97:741–747.
- Bajuk P., Babnik B., Snoj K., Milčinski T., Pislak Ocepek L., Škof M. Coumaphos residues in honey, bee brood, and beeswax after Varroa treatment. Apidologie. 2017;48:588–598.
- Belles X. Beyond Drosophila: RNAi in vivo and functional genomics in insects. Annual Review of Entomology. 2010;55:111–128.
- Bortolin, F.; Rigato, E.; Perandin, S.; Granato, A.; Zulian, L.; Millino, C.; Pacchioni, B.; Mutinelli, F.; Fusco, G. First evidence of the effectiveness of a field application of RNAi technology in reducing infestation of the mite Varroa destructor in the western honey bee (Apis mellifera). Parasites & Vectors 2025, 18 (1), 28. doi: 10.1186/s13071-025-06673-7
- Campbell E.M., Budge G.E., Bowman A.S. Gene-knockdown in the honey bee mite Varroa destructor by a non-invasive approach: studies on a glutathione S-transferase. Parasites & Vectors. 2010;3:73.
- Campbell E.M., Budge G.E., Watkins M., Bowman A.S. Transcriptome analysis of the synganglion from the honey bee mite Varroa destructor and RNAi knockdown of neural peptide targets. Insect Biochemistry and Molecular Biology. 2016;70:116–126.
- Chen A., Zheng W., Zhang H. Effects of RNA interference targeting Bactrocera dorsalis ds-Bdrpl19 on rpl19 expression in nontarget insects. Ecotoxicology. 2015;24:595–603.
- Chen J., Peng Y., Zhang H., Wang K., Tang Y., Gao J., et al. Transcript level as a key factor affecting RNAi efficiency. Pesticide Biochemistry and Physiology. 2021;176:104872.
- Christiaens O., Dzhambazova T., Kostov K., Arpaia S., Joga M.R., Urru I., et al. Literature review of baseline information on RNAi to support environmental risk assessment of RNAi-based GM plants. EFSA Supporting Publications. 2018;15:EN-1424.
- Delaplane K.S., Dag A., Danka R.G., Freitas B.M., Garibaldi L.A., Goodwin R.M., et al. Standard methods for estimating strength parameters of Apis mellifera colonies. Journal of Apicultural Research. 2013;52:1–12.
- Desai S.D., Eu Y.J., Whyard S., Currie R.W. Reduction in deformed wing virus infection in larval and adult honey bees by double-stranded RNA ingestion. Insect Molecular Biology. 2012;21:446–455.
- Di Prisco G., Annoscia D., Margiotta M., Ferrara R., Varricchio P., Zanni V., et al. Mutualistic symbiosis between a parasitic mite and a pathogenic virus undermines honey bee immunity. PNAS. 2016;113:3203–3208.
- Di Prisco G., Cavaliere V., Annoscia D., Varricchio P., Caprio E., Nazzi F., et al. Neonicotinoid clothianidin impairs insect immunity and enhances viral replication. PNAS. 2013;110:18466–18471.
- Ding T., Wang S., Gao Y., Li C., Wan F., Zhang B. Toxicity and effects of four insecticides on Na⁺/K⁺-ATPase of Frankliniella occidentalis. Ecotoxicology. 2020;29:58–64.
- Fletcher S.J., Reeves P.T., Hoang B.T., Mitter N. A perspective on RNAi-based biopesticides. Frontiers in Plant Science. 2020;11:51.
- Fries I., Imdorf A., Rosenkranz P. Survival of Varroa-infested colonies in a Nordic climate. Apidologie. 2006;37:564–570.
- Garbian Y., Maori E., Kalev H., Shafir S., Sela I. Bidirectional transfer of RNAi between honey bee and Varroa destructor: mite gene silencing reduces Varroa populations. PLoS Pathogens. 2012;8:e1003035.
- Genersch E., Von Der Ohe W., Kaatz H., Schroeder A., Otten C., Büchler R., et al. The German bee monitoring project: long-term analysis of winter colony losses. Apidologie. 2010;41:332–352.
- González-Cabrera J., Bumann H., Rodríguez-Vargas S., Kennedy P.J., Krieger K., Altreuther G., et al. A single mutation drives pyrethroid resistance in Varroa destructor. Journal of Pest Science. 2018;91:1137–1144.
- Hernández-Rodríguez C.S., Magín Ó., Calatayud F., Mahiques M.J., Mompó A., Segura I., et al. Large-scale monitoring of resistance to coumaphos, amitraz, and pyrethroids in Varroa destructor. Insects. 2021;12:27.
- Hollowell H., Rieske L.K. Southern pine beetle-specific RNAi shows no effect on model nontarget insects. Journal of Pest Science. 2022;95:1429–1441.
- Huang Q., Chen Y., Neumann P., Li W., Evans J.D. Silencing of Dicer reduces Nosema ceranae spore loads. Fungal Genomics & Biology. 2016;6:1–4.
- Hunter W., Ellis J., Vanengelsdorp D., Hayes J., Westervelt D., Glick E., et al. Large-scale field application of RNAi reducing IAPV disease in honey bees. PLoS Pathogens. 2010;6:e1001160.
- Imdorf A., Buehlmann G., Gerig L., Kilchenmann V., Wille H. Evaluation of methods for estimating brood area and worker populations. Apidologie. 1987;18:137–146.
- Kleter G.A. Food safety assessment of crops engineered with RNAi. Pest Management Science. 2020;76:3333–3339.
- Lee K.V., Moon R.D., Burkness E.C., Hutchison W.D., Spivak M. Practical sampling plans for Varroa destructor. Journal of Economic Entomology. 2010;103:1039–1050.
- Leonard S.P., Powell J.E., Perutka J., Geng P., Heckmann L.C., Horak R.D., et al. Engineered symbionts activate honey bee immunity and limit pathogens. Science. 2020;367:573–576.
- Liu X., Zhang Y., Yan X., Han R. RNAi prevention of Chinese Sacbrood Virus in Apis cerana. Current Microbiology. 2010;61:422–428.
- Lümmen P., Khajehali J., Luther K., Van Leeuwen T. Spirotetramat inhibits acetyl-CoA carboxylases. Insect Biochemistry and Molecular Biology. 2014;55:1–8.
- Macedo P.A., Wu J., Ellis M.D. Use of inert dusts for detecting and assessing Varroa infestations. Journal of Apicultural Research. 2002;41:3–7.
- Mancuso T., Croce L., Vercelli M. Brood removal and biotechniques for sustainable control of Varroa: economic impact. Sustainability. 2020;12:2302.
- Maori E., Garbian Y., Kunik V., Mozes-Koch R., Malka O., Kalev H., et al. A transmissible RNA pathway in honey bees. Cell Reports. 2019;27:1949–1959.
- Maori E., Paldi N., Shafir S., Kalev H., Tsur E., Glick E., et al. Silencing IAPV via dsRNA ingestion. Insect Molecular Biology. 2009;18:55–60.
- McGruddy R.A., Smeele Z.E., Manley B., Masucci J.D., Haywood J., Lester P.J. RNAi as a next-generation control for suppressing Varroa reproduction. Pest Management Science. 2024;80:4770–4778.
- Morfín N., Goodwin P.H., Guzman-Novoa E. Varroa destructor and its impacts on honey bee biology. Frontiers in Bee Science. 2023;1:1272937.
- Noël A., Le Conte Y., Mondet F. Varroa destructor: mechanisms of harm and mitigation strategies. Emerging Topics in Life Sciences. 2020;4:45–57.
- Paldi N., Glick E., Oliva M., Zilberberg Y., Aubin L., Pettis J. Effective gene silencing in a microsporidian parasite of honey bees. Applied and Environmental Microbiology. 2010;76:5960–5964.
- Parker K.M., Borrero V.B., Van Leeuwen D.M., Lever M.A., Mateescu B., Sander M. Environmental fate of dsRNA in soils. Environmental Science & Technology. 2019;53:3027–3036.
- Powell M.E., Bradish H.M., Gatehouse J.A., Fitches E.C. Systemic RNAi in the small hive beetle. Pest Management Science. 2017;73:53–63.
- Rosenkranz P., Aumeier P., Ziegelmann B. Biology and control of Varroa destructor. Journal of Invertebrate Pathology. 2010;103:S96–S119.
- Schiemann J., Dietz-Pfeilstetter A., Hartung F., Kohl C., Romeis J., Sprink T. Risk assessment and regulation of plants modified by modern biotechniques. Annual Review of Plant Biology. 2019;70:699–726.
- Shang X.F., Miao X.L., Dai L.X., Wang Y., Li B., Pan H., Zhang J.Y. Acaricidal activity of strophanthidin derivatives and inhibition of Na⁺/K⁺-ATPase. Veterinary Parasitology. 2021;296:109498.
- Straub L., Williams G.R., Vidondo B., Khongphinitbunjong K., Retschnig G., Schneeberger A., et al. Synergistic impacts of neonicotinoids and mites on honey bees. Scientific Reports. 2019;9:8159.
- Tan J., Levine S.L., Bachman P.M., Jensen P.D., Mueller G.M., Uffman J.P., et al. No impact of DvSnf7 RNA on honey bee adults and larvae. Environmental Toxicology and Chemistry. 2016;35:287–294.
- Wilson R.C., Doudna J.A. Molecular mechanisms of RNA interference. Annual Review of Biophysics. 2013;42:217–239.
- Yoo M.S., Truong A.T., Jeong H., Hahn D.H., Lee J.S., Yoon S.S., et al. Large-scale dsRNA application for reducing Sacbrood virus in Apis cerana. Viruses. 2023;15:897.
- Zhou H., Zhang Y.Q., Lai T., Wang D., Liu J.L., Guo F.Y., et al. Chitinase gene silencing increases susceptibility of Tetranychus cinnabarinus to scopoletin. BioMed Research International. 2017:9579736.
- Zhu K.Y., Palli S.R. Mechanisms, applications, and challenges of insect RNA interference. Annual Review of Entomology. 2020;65:293–311.
Новость подготовили
© д.б.н., в.н.с. Ильясов Рустем Абузарович, Ильясова Алла Юрьевна
18.12.2025