Generation of iPSC-Derived iNKT Cells with Pro-Hematopoietic Activity.
Stem Cell Rev Rep. 2025 Dec 11. doi: 10.1007/s12015-025-11031-2
 © Шевелева Ольга Николаевна, научный сотрудник,кандидат биологических наук.
© Шевелева Ольга Николаевна, научный сотрудник,кандидат биологических наук.Область научных интересов: клеточная биология, гемопоэтические стволовые клетки, внеклеточные везикулы,
клетки-супрессоры миелоидного происхождения (МДСК), генерация МДСК in vitro.
T-клеточная терапия набирает популярность как персонализированный подход к лечению рака, где используются собственные иммунные клетки пациента. Т-лимфоциты извлекаются, "перепрограммируются" для распознавания и атаки раковых клеток, а затем вводятся обратно в организм. Это позволяет иммунной системе пациента целенаправленно бороться с опухолью, что особенно эффективно при таких заболеваниях крови, как лейкозы и лимфомы.
В настоящее время Т-клеточная терапия в основном связана с получением Т-клеток из периферической крови пациента, их активацией, экспансией или генетическими манипуляциями ex vivo и введением обратно пациенту. Такая стратегия является дорогостоящей, трудоемкой и очень зависит от качества Т-клеток пациента, которое часто бывает неудовлетворительным из-за самого заболевания или побочных эффектов терапии, например, иммуносупрессии. Получение Т-клеток из индуцированных плюрипотентных стволовых клеток (иПСК) человека является относительно новым, но достаточно перспективным подходом, хоть и не лишённым пока таких минусов, как получение функционально незрелых Т-клеток в условиях in vitro и необходимости применения ксеногенных фидерных клеток (обычно, линии OP9).
Особый интерес в Т-клеточной иммунотерапии привлекают инвариантные естественные киллерные Т-клетки (iNKT-клетки). iNKT – это особая клеточная популяция, играющая важную роль в быстром иммунном ответе. В отличие от большинства Т-клеток, которые распознают антигены, связанные с молекулами MHC, iNKT-клетки распознают липиды и гликолипиды, представленные неклассическими CD1d-антигенпрезентирующими молекулами (1). iNKT-клетки не нуждаются в предварительном прайминге, в отличие от обычных Т-клеток, и быстро выполняют эффекторные функции после стимуляции, включая выработку широкого спектра цитокинов, опосредование противоопухолевой активности посредством цитолиза и т.д. Интересны и сообщения об участии iNKT-клеток в гемопоэтической дифференцировке (2). Еще одна особенность iNKT-клеток заключается в том, что они не вызывают аллогенные ответы и могут использоваться для иммунотерапии без риска развития реакции «трансплантат против хозяина» (РТПХ). Все это в совокупности делает iNKT-клетки очень привлекательными для их потенциального применения в клеточной иммунотерапии (3). Сложность заключается в маленьком количестве этих клеток в крови (в среднем 0,1-0,3% от Т-клеток) и трудности их выделения без загрязнения конечной популяции обычными Т-клетками, которые могут вызвать иммунный ответ при введении. В связи с этим, вышедшее в 2025 году исследование, представленное Кумаром и соавторами (группа И. Слуквина), вызывает особый интерес поскольку авторам удалось при минимальном использовании фидерных клеток получить функционально активные iNKT.
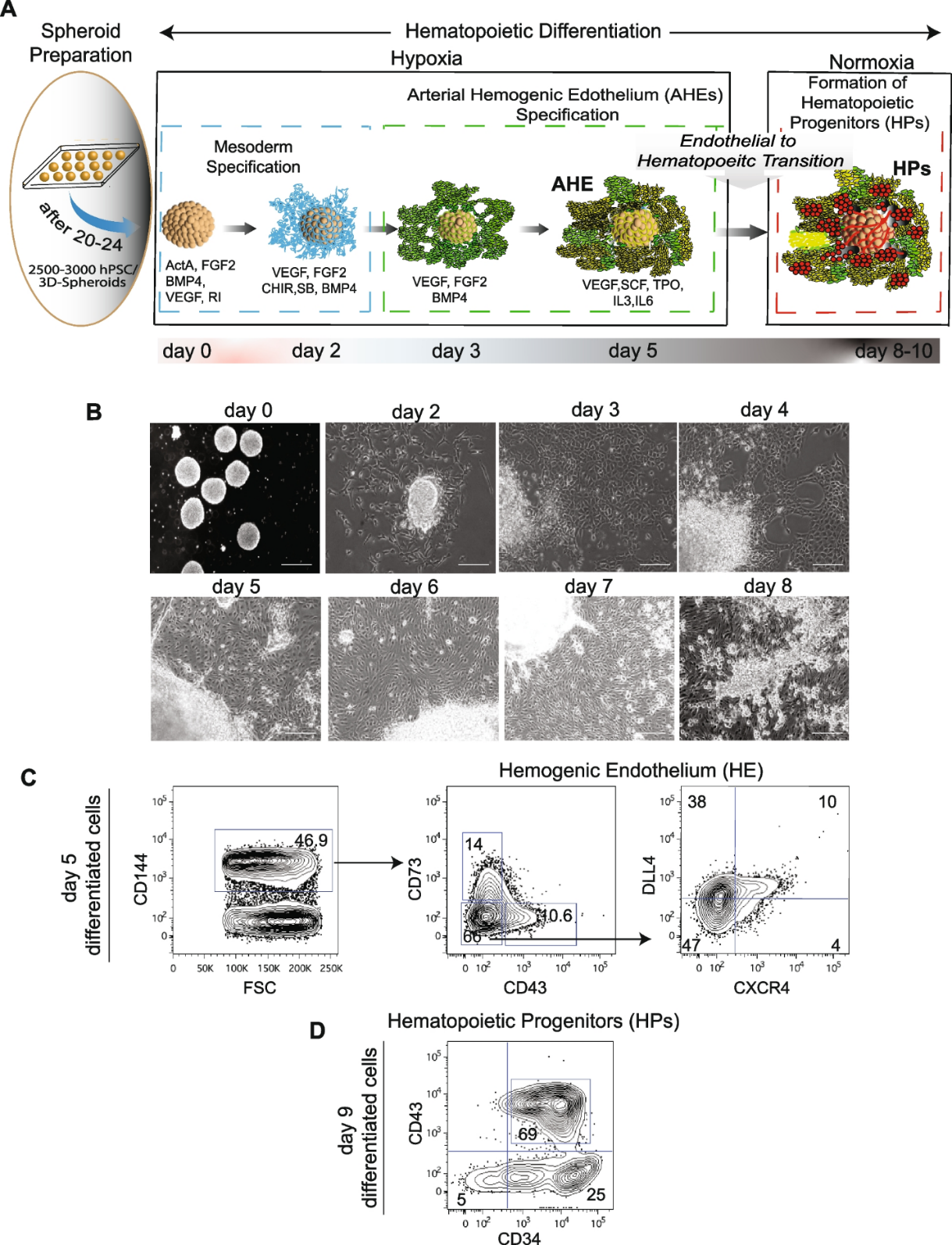
В рассматриваемой работе, 2025-го года, авторы разработали протокол для получения иПСК из соматических iNKT-клеток и их дифференцировки в i-iNKT-клетки с активностью, поддерживающей гемопоэз. На первом этапе работы для генерации иПСК авторы применяли набор, содержащий вирусы Сендай, несущие основные факторы плюрипотентности Oct4, Sox2, Klf4 и c-Myc, которыми осуществляли перепрограммирование предварительно отсортированных CD4 + iNKT-клеток человека. Помимо общей характеристики, важным моментом было показать, что полученные линии иПСК содержат перестройку рецепторов TCR (Т-клеточные рецепторы), типичную для iNKT-клеток. Второй этап работы подразумевал генерацию гемопоэтических предшественников CD34 + из иПСК. На этом этапе авторы получали в висячих каплях 3D-сфероиды и дифференцировали их в среде с добавлением различных факторов (см. рис 1). Благодаря оптимизации концентрации ингибитора WNT-сигнализации (CHIR99021) и ингибитора TGFβ-сигнализации (SB-431542) авторам удалось добиться увеличения количества клеток гемогенного эндотелия (количество DLL4 + CXCR4 ± достигало 50% от общего числа клеток). А на 9-й день дифференцировки около 60% собранных плавающих гемопоэтических предшественников были CD34+CD43+.
Рисунок 1. Гемопоэтическая дифференцировка иПСК, полученных из iNKT-клеток (рисунок из оригинальной статьи Kumar et al., 2025, doi: 10.1007/s12015-025-11031-2)
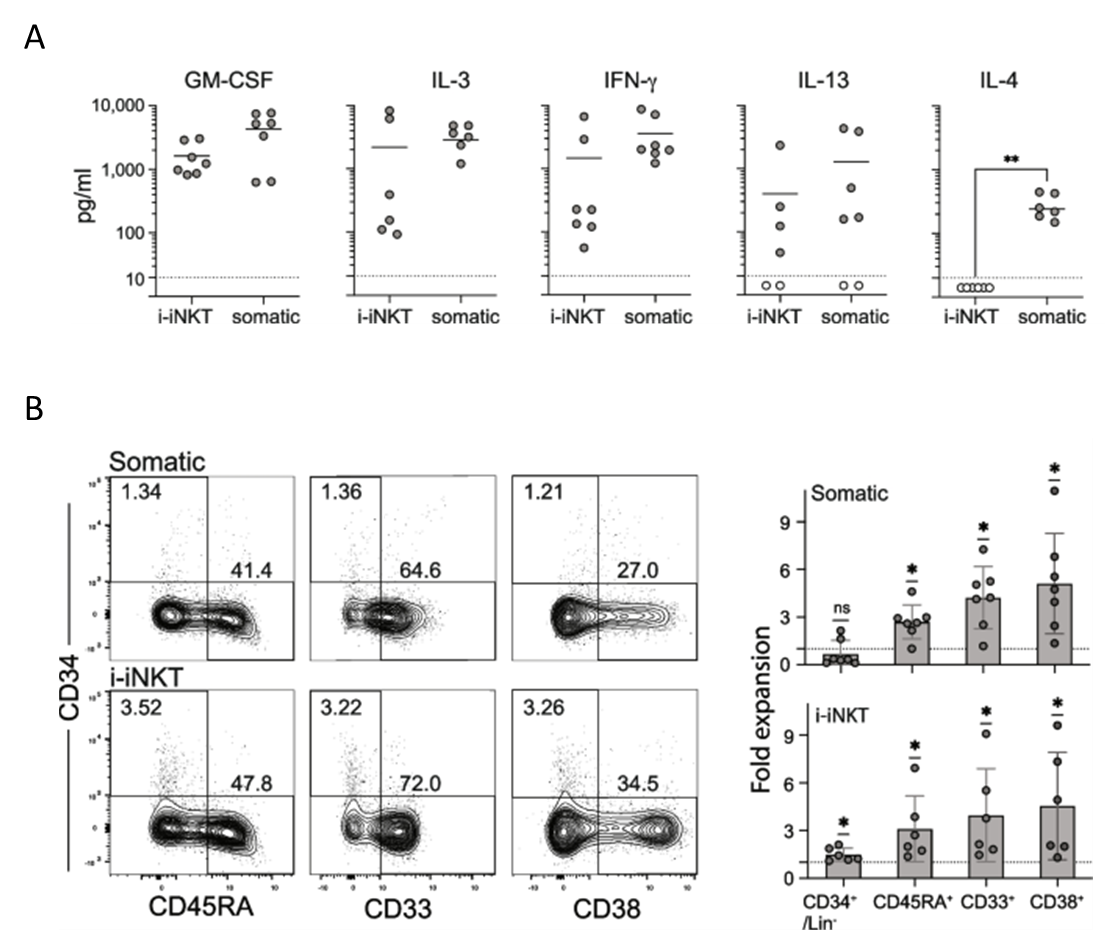
Для получения iNKT-клеток авторы культивировали собранные гемопоэтические предшественники CD34 + на фидерных клетках OP9, экспрессирующих человеческий лиганд NOTCH DLL4 (OP9-DLL4), в среде c факторами – SCF, IL-7, FLT3L. После дальнейшего культивирования в среде, содержащей IL-2, в течение дополнительных 7 дней, почти 100% полученных i-iNKT клеток экспрессировали CD45 и CD3 на уровнях, аналогичных соматическим iNKT-клетками. Полученные i-iNKT проявляли и свойства соматических iNKT-клеток: сходную экспрессию транскрипционных факторов, продукцию цитокинов (за исключением IL-4, см. рис 2B), аналогичным образом связывали человеческий тетрамер CD1d, нагруженный антигенным липидом α-галактозилцерамидом (α-GalCer), демонстрировали сходные функциональные свойства.
Интересно, что i-iNKT-клетки демонстрировали гемопоэтическую активность, как и соматические iNKT-клетки, благодаря продукции ими GM-CSF и IL-3. Культивирование i-iNKT в transwell-системе с CD34 + клетками из пуповинной крови человека приводило к стимуляции пролиферации, как CD34 + клеток, так и различных кроветворных предшественников CD45RA+, CD33+ и CD38+ (рис 2B).
Приведенное в данной работе исследование имеет большой потенциал для дальнейшего применения i-iNKT-клеток в качестве терапевтического средства во время трансплантации гемопоэтических стволовых клеток (ГСК). В будущем авторы планируют изучать способны ли i-iNKT-клетки, полученные из соматической линии CD4 +iNKT-клеток, также как iNKT снижать риск развития РТПХ, сохраняя при этом противоопухолевый ответ донорских Т-клеток и способствуя приживлению гемопоэтических клеток.
Рисунок 2. iNKT-клетки из иПСК (i-iNKT-клетки) демонстрировали свойства, сравнимые с соматическими iNKT-клетками: А - продукцию цитокинов после стимуляции анти-CD3 (результаты ИФА) и В – гемопоэтическую активность, определяемую при сравнении количества гемопоэтических клеток после 14 дней культивирования CD34 + клеток из пуповинной крови и 7 дней воздействия на них i-iNKT-клеток или соматических iNKT-клеток. Значения p < 0,05 обозначены звездочкой * (рисунок из оригинальной статьи Kumar et al., 2025, doi: 10.1007/s12015-025-11031-2)
Список литературы:
1. Kawano, T., Cui, J., Koezuka, Y., Toura, I., Kaneko, Y., Motoki, K., Ueno, H., Nakagawa, R., Sato, H., Kondo, E., Koseki, H., & Taniguchi, M. (1997). CD1d-restricted and TCR-mediated activation of valpha14 NKT cells by glycosylceramides. Science, 278, 1626–1629
2. Kotsianidis I, Silk JD, Spanoudakis E, Patterson S, Almeida A, Schmidt RR, Tsatalas C, Bourikas G, Cerundolo V, Roberts IA, Karadimitris A. Regulation of hematopoiesis in vitro and in vivo by invariant NKT cells. Blood. 2006 Apr 15;107(8):3138-44. doi: 10.1182/blood-2005-07-2804
3. Iinuma, T., Kurokawa, T., Aoki, T. et al. Allogeneic iPSC-derived iNKT cells in recurrent head and neck cancer: a phase 1 trial. Nat Commun 16, 11666 (2025). https://doi.org/10.1038/s41467-025-66801-w
Новость подготовила
© Шевелева Ольга Николаевна, кандидат биологических наук
17.02.2026