Taxonomically different symbiotic communities of sympatric Arctic sponge species show functional similarity with specialization at species level. mSystems 0:e01147-25.
https://journals.asm.org/doi/10.1128/msystems.01147-25

Научные интересы: клеточная пластичность, протеомика, гомеостаз клеточного протеома,
регенерация, металлопротеины, симбиотические бактерии

соискатель ИБР РАН им. Н.К.Кольцова.
Научные интересы: микробиология, биоинформатика.
Морские губки являются одними из самых древних многоклеточных организмов и представляют собой один из первых примеров симбиоза между животными и бактериями. Бактерии, археи, эукариоты и вирусы вместе с губкой образуют холобионт — единую функциональную систему, в которой каждый участник вносит свой вклад в стабильность и гомеостаз организма [1]. Бактериальные симбионты играют важную роль в защите хозяина от патогенов, обеспечении его витаминами, аминокислотами и другими метаболитами, а также участвуют в регуляции циклов азота и серы [2]. Благодаря этому губки способны обитать в крайне бедных питательными веществами водах, где они формируют устойчивые микроэкосистемы.
Изучение симбиоза губок с микроорганизмами помогает не только понять ранние этапы эволюции многоклеточных животных, но и выявить новые метаболические пути, потенциально значимые для биотехнологии. Методы высокопроизводительного секвенирования (NGS) позволили исследовать эти ассоциации у организмов, обитающих в экстремальных условиях, таких как арктические моря, где температура воды и доступность органического вещества ограничивают большинство форм жизни. Несмотря на растущий интерес, многие виды полярных губок остаются слабо охарактеризованными, а механизмы формирования их микробных сообществ и функциональной специализации до сих пор изучены недостаточно.
Наша работа охватывает данные за шесть лет наблюдений (2016, 2018 и 2022 годы) и демонстрирует уникальную таксономическую организацию ассоциированных микробных сообществ трёх симпатрических холодноводных губок — Halichondria panicea, Halichondria sitiens и Isodictya palmata, обитающих Кандалакшском заливе Белого моря. Микробиомы двух последних видов были описаны впервые.
Основные результаты исследования
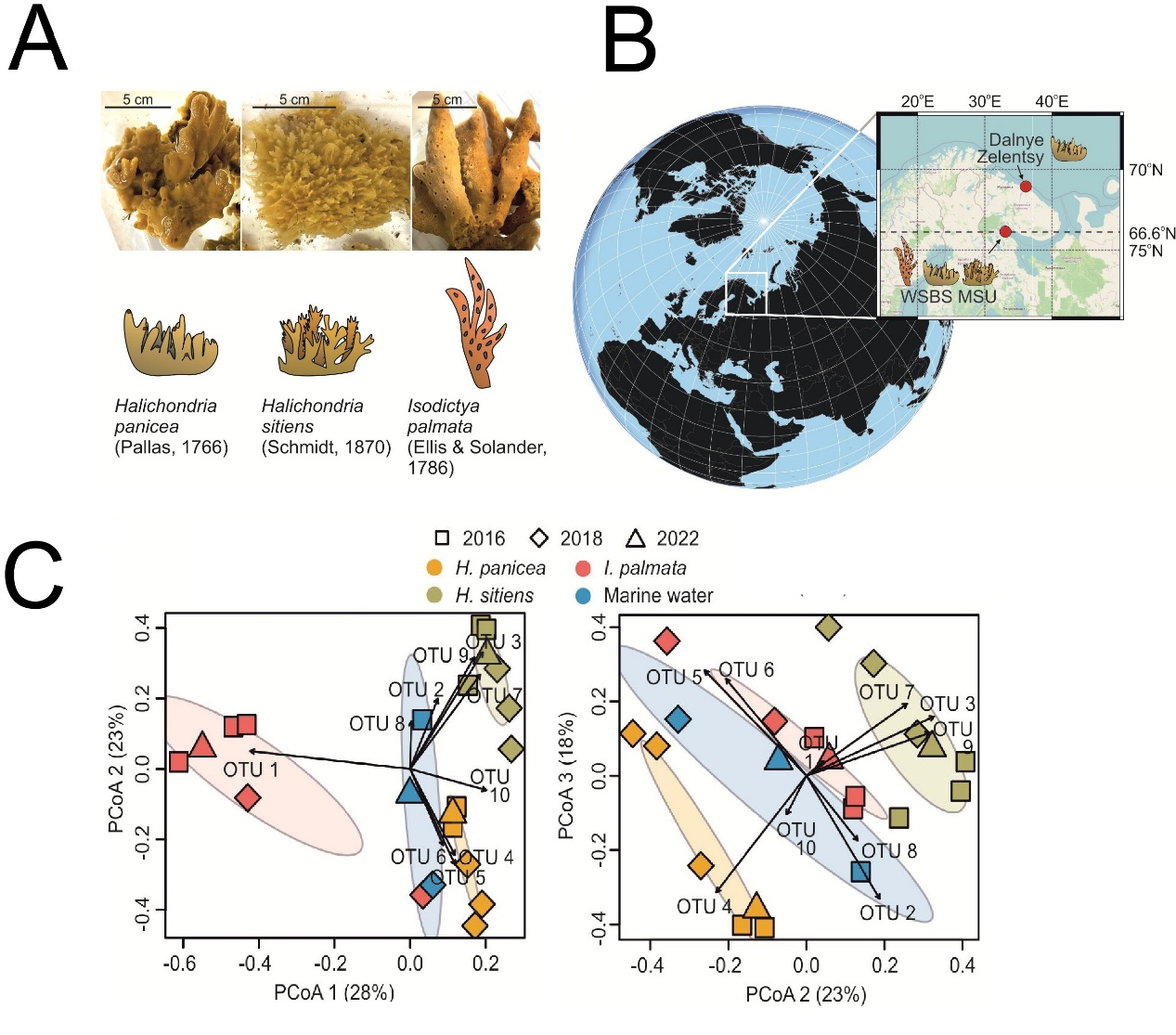
Все три вида губок обладали видоспецифичными микробными сообществами, даже несмотря на совместное обитание в одном арктическом биотопе. Симбионты относились преимущественно к классам Alphaproteobacteria и Gammaproteobacteria. Таким образом, каждая губка имела уникальный «микробный паспорт», отражающий особенности её физиологии и, вероятно, эволюционной истории (Рисунок 1).
Рисунок 1. А - Репрезентативные изображения трёх изученных видов губок. Масштабная линейка составляет 5 см. Под соответствующими изображениями показаны графические значки, иллюстрирующие виды губок. B - Карта мест сбора образцов. С - Анализ главных координат (PCoA) различий по Брэй–Кёртису между микробиомами губок и морской воды Белого моря.
Несмотря на таксономические различия, функциональный потенциал микробиомов оказался сходным. Все три сообщества кодировали гены, участвующие в биосинтезе аминокислот, витаминов и кофакторов, а также транспортных систем, обеспечивающих их доставку хозяину. Симбионты также обладали потенциалом к деградации сложных органических соединений, что позволяет рассматривать их как ключевых участников переработки органического вещества в арктических экосистемах. Эти данные подтверждают идею функциональной конвергенции симбионтов: разные бактериальные таксоны способны обеспечивать сходные метаболические функции в рамках одного экологического контекста.
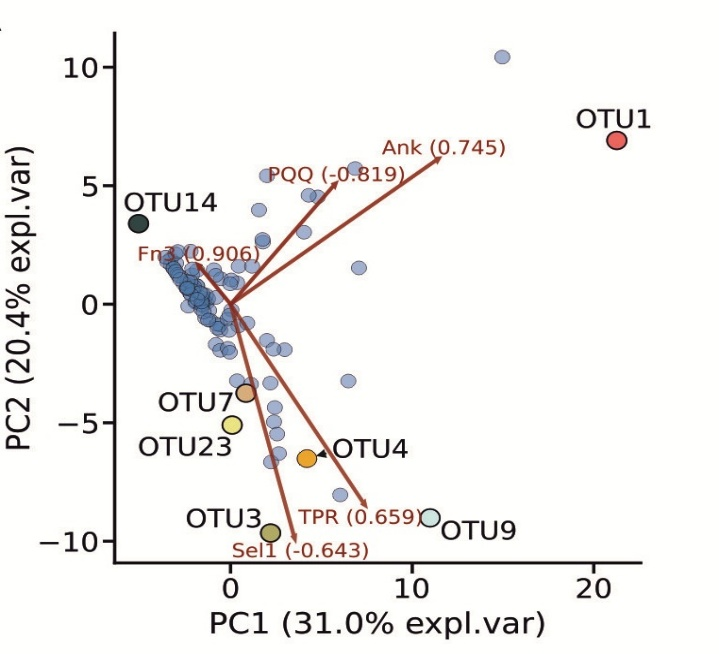
При этом на уровне отдельных симбионтов выявлены различия в составе эукариот-подобных белков (ELPs), которые, вероятно, обеспечивают специфическое узнавание и поддержание стабильного взаимодействия между бактерией и губкой, предотвращая фагоцитоз симбионта (Рисунок 2) [3].
Рисунок 2. Биплот PCA нормализованных частот доменов ELP в геномах симбионтов (отмеченные точки) и контрольных метагеномных бинах (синие точки), реконструированных из метагеномных микробиомов губок и морской воды. Число в скобках указывает на нагрузку признаков на главный компонент.
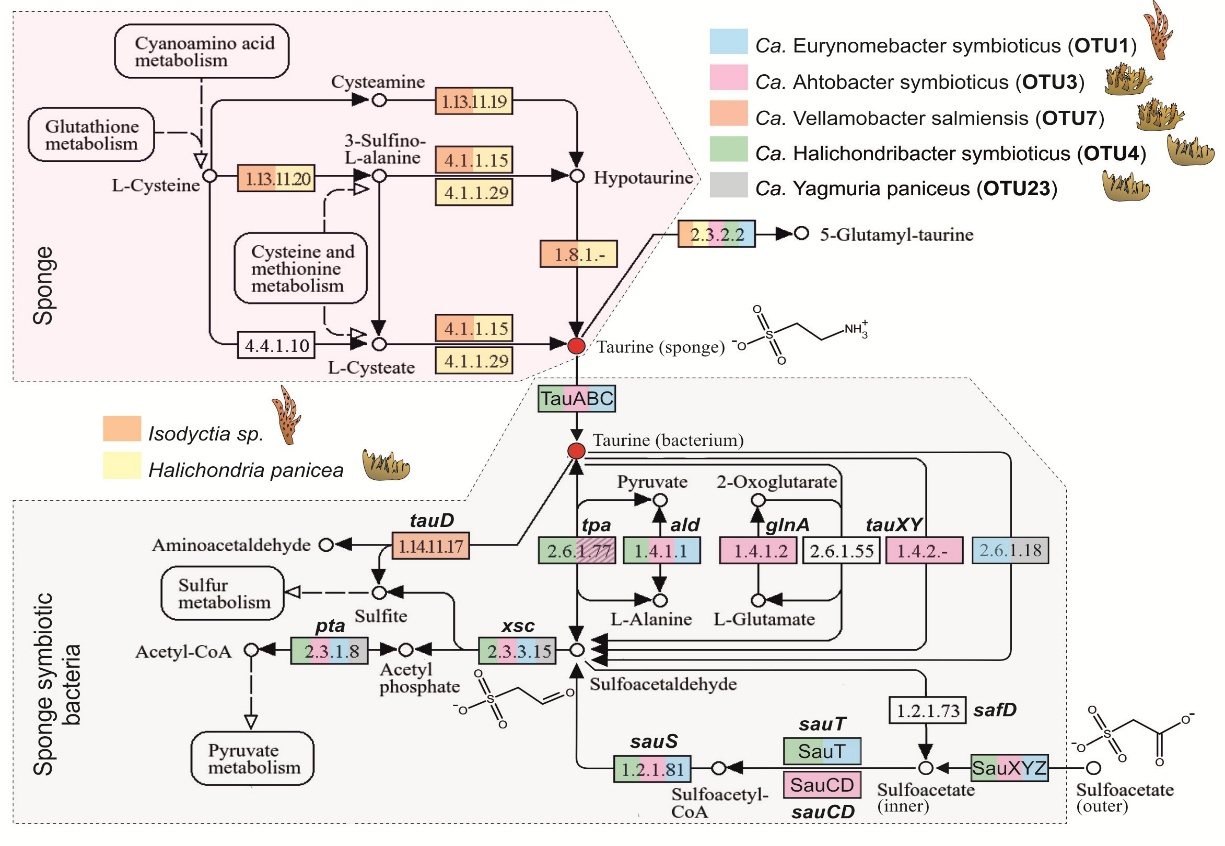
Особое внимание заслуживает обнаружение путей метаболизма таурина и сульфоацетата — они были выявлены исключительно у доминантных симбионтов всех трёх губок (Рисунок 3). Эти соединения могут использоваться как дополнительные источники углерода, серы и энергии [4]. Более того, гены, связанные с транспортом и метаболизмом сульфоацетата, рассматриваются авторами как потенциально новый симбиотический признак, обеспечивающий конкурентное преимущество определённых бактериальных линий.
Рисунок 3. Метаболическая схема синтеза и деградации таурина и сульфоацетата по данным KEGG. Заштрихованный участок, соответствующий гену tpa в геноме симбионта OTU3, указывает на то, что этот ген присутствовал в нескольких исходных метагеномных биннах OTU3, но отсутствовал в итоговой сборке генома OTU3.
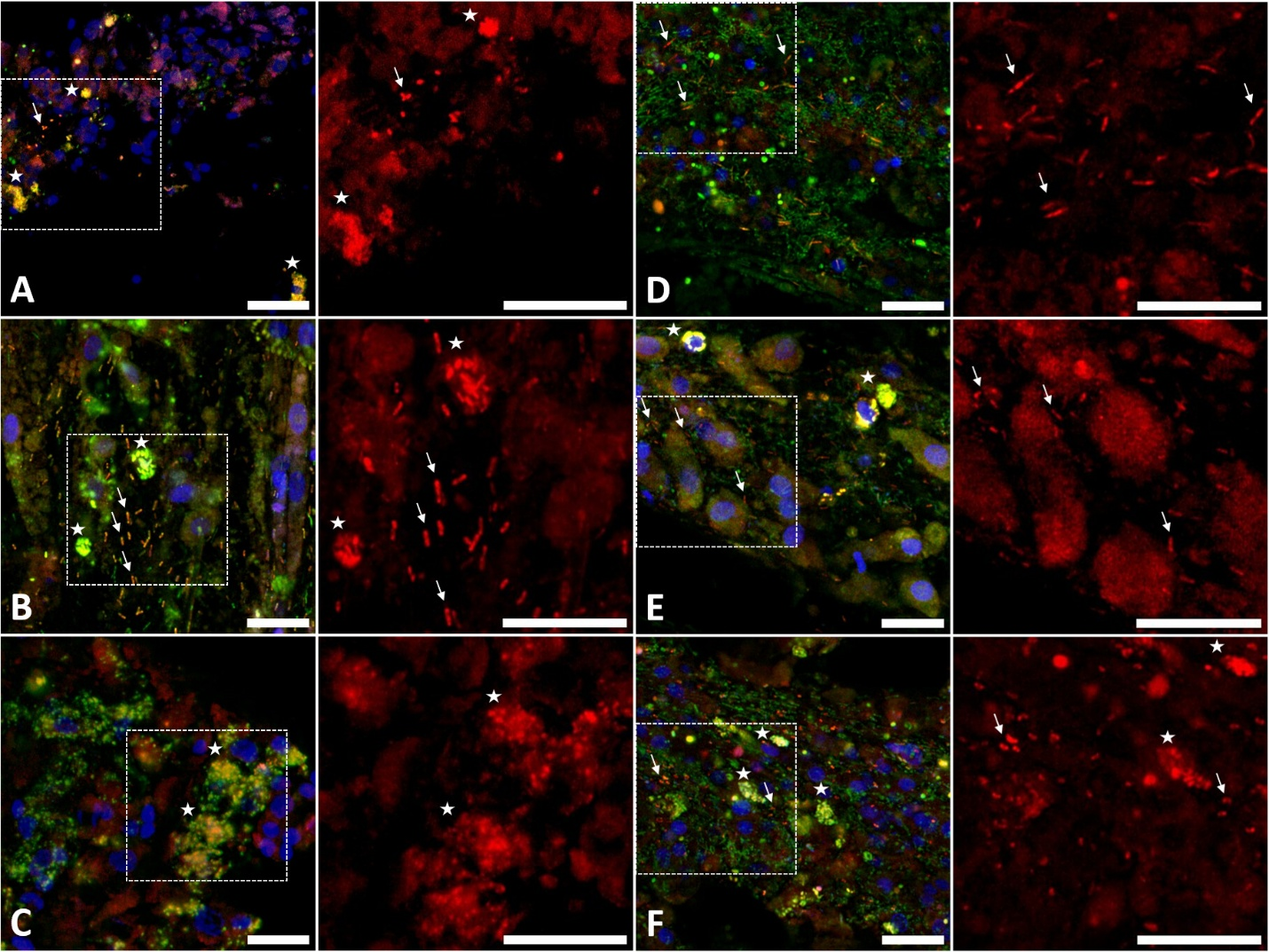
Для подтверждения локализации симбиотических бактерий авторы применили флуоресцентную гибридизацию in situ (FISH). Анализ показал, что большинство доминантных бактерий располагаются не в каналах водоносной системы, где происходит активное движение воды, а в мезохиле — рыхлой соединительнотканной матрице, заполняющей промежутки между пинакодермой и хоанодермой. Такая пространственная организация указывает на стабильное включение этих бактерий в состав холобионта, а не на их случайное поступление с током воды при фильтрации (Рисунок 4).
Рисунок 4. Изображения FISH бактериальных клеток в тканевых срезах исследованных губок. Бактерии окрашены с помощью зонда, специфичного к симбиотическим бактериям, меченного Cy3 (красный), и универсальных зондов с меткой Cy5 (зелёный). ДНК окрашена Hoechst 33342 (синий).
(A) — срез H. panicea, гибридизованный с зондом, специфичным для OTU4; (B) — срез H. sitiens, зонд для OTU3; (C) — срез I. palmata, зонд для OTU1; (D) — срез H. sitiens, зонд для OTU7; (E) — срез H. sitiens, зонд для OTU9; (F) — срез H. sitiens, зонд для OTU14. Слева показано объединённое изображение трёх цветовых каналов, справа — увеличенный участок, обозначенный белым прямоугольником, в красном канале (Cy3). Стрелки и звёздочки указывают отдельные бактериальные клетки и их скопления соответственно. Масштабная линейка — 10 мкм.
Долгосрочные наблюдения показали относительную устойчивость микробных сообществ во времени, за исключением 2018 года, когда в Белом море наблюдались аномально высокие температуры воды и массовая гибель губок [5, 6]. В этот период микробиомы претерпели заметные сдвиги в составе и относительных пропорциях таксонов, что, вероятно, отражало стресс-индуцированные перестройки симбиотических связей. К 2022 году микробные сообщества восстановили исходную структуру, демонстрируя высокую, хотя и не абсолютную, резистентность к внешним стрессам. Эти результаты подчёркивают уязвимость арктических губочных экосистем в условиях глобального потепления и возможные долгосрочные последствия для биоразнообразия полярных морей.
Таким образом, полученные данные подтверждают, что видоспецифичные микробные сообщества губок Белого моря сохраняют функциональное сходство при таксономической разобщённости. Это отражает конвергентную эволюцию микробиомов на уровне метаболических функций и подчёркивает высокую степень адаптации и специализации их членов. Уникальные симбиотические признаки, выявленные у арктических губок, делают их перспективными объектами для дальнейшего изучения устойчивости и коэволюции симбиозов в экстремальных условиях.
1. Stévenne C, Micha M, Plumier J-C, Roberty S. 2021. Corals and sponges under the light of the holobiont concept: how microbiomes underpin our understanding of marine ecosystems. Front Mar Sci 8.
2. Pita L, Rix L, Slaby BM, Franke A, Hentschel U. 2018. The sponge holobiont in a changing ocean: from microbes to ecosystems. Microbiome 6:46.
3. Reynolds D, Thomas T. 2016. Evolution and function of eukaryotic-like proteins from sponge symbionts. Mol Ecol 25:5242–5253.
4. Moeller FU, Herbold CW, Schintlmeister A, Mooshammer M, Motti C, Glasl B, Kitzinger K, Behnam F, Watzka M, Schweder T, Albertsen M, Richter A, Webster NS, Wagner M. 2023. Taurine as a key intermediate for host-symbiont interaction in the tropical sponge Ianthella basta. ISME J 17:1208–1223.
5. Rusanova A, Fedorchuk V, Toshchakov S, Dubiley S, Sutormin D. 2022. An interplay between viruses and bacteria associated with the white sea sponges revealed by metagenomics. Life 12:25.
6. Ereskovsky A, Ozerov DA, Pantyulin AN, Tzetlin AB. 2019. Mass mortality event of White Sea sponges as the result of high temperature in summer 2018. Polar Biol 42:2313–2318.
Новость подготовил
© кандидат биологических наук, научный сотрудник Финошин Александр Дмитриевич
16.11.2025