https://pmc.ncbi.nlm.nih.gov/articles/PMC12791003/

Область научных интересов: нейроэтология,нейробиология, нейротрансмиттеры, поведение.
Мобильные элементы, в частности, семейство LINE-1 или L1 (long interspersed nuclear element) составляют существенную часть генома человека. Традиционно их рассматривают как генетических «паразитов» или «мусорную ДНК», чья мобильность угрожает целостности генома, что требует их эпигенетического сайленсинга. Однако, в последние годы накапливаются данные, что в раннем эмбриогенезе млекопитающих некоторые L1 экспрессируются и могут выполнять регуляторные функции, хотя конкретные механизмы и их значение для человека оставались малоизученными.
Основная проблема в исследовании L1 заключается в огромном количестве этих повторов в геноме и их гетерогенности, что затрудняет анализ на уровне индивидуальных геномных локусов. Большинство работ рассматривало L1 как монолитное семейство. Данное исследование ставит целью преодолеть это ограничение, чтобы выяснить, как конкретные, эволюционно молодые L1 влияют на транскрипционные сети в плюрипотентных стволовых клетках человека и в ходе раннего нейрогенеза, используя модель церебральных органоидов.
В индуцированных плюрипотентных стволовых клетках (иПСК) человека активно экспрессируются тысячи уникальных локусов, принадлежащих к человеко-специфичным (L1HS) и гоминоид-специфичным (L1PA2, L1PA3) подсемействам. Их экспрессия строго коррелирует с характерным активным эпигенетическим ландшафтом: отсутствием метилирования ДНК в промоторной области и наличием маркера активных промоторов — гистоновой метки H3K4me3. Данные подтверждают, что активность L1 в плюрипотентных клетках обусловлена их способностью ускользать от репрессии, в отличие от других транспозонов. Это возможно из-за эволюционных изменений в последовательностях, мешающих связыванию репрессорных комплексов (например, KRAB-ZFP).
Для функционального исследования была оптимизирована высокоточная система CRISPR-интерференции (CRISPRi), направленная на 5'-нетранслируемую область (5' UTR) полноразмерных L1. Подход обеспечил эффективное и специфичное подавление транскрипции целевых элементов, что подтверждалось потерей как L1-РНК, так и белка, а также заменой активной гистоновой метки H3K4me3 на репрессивную H3K9me3 непосредственно в сайтах связывания гидовой РНК. Использование CRISPRi, нацеленной на 5' UTR, позволило селективно подавить только полнодлинные, транскрипционно активные L1, минимизировав побочные эффекты на многочисленные усечённые и встроенные в гены копии. Это обеспечило высокую специфичность вмешательства по сравнению с методами, нацеленными на консервативные кодирующие области (ORF1/ORF2).
Несмотря на почти полное отключение L1, иПСК сохраняли пролиферацию, экспрессию ключевых маркеров плюрипотентности (OCT4, NANOG, SOX2) и способность к дифференцировке во все три зародышевых листка. Это демонстрирует, что в иПСК человека L1 не обязательны для поддержания плюрипотентного состояния. Однако их подавление привело к снижению экспрессии около 100 соседних генов, из которых треть кодировала белки.
Детальный анализ показал, что L1 влияют на эти гены по цис-регуляторному механизму, выступая в роли альтернативных промоторов или энхансеров. В частности, антисмысловой промотор L1 инициирует транскрипцию химерных РНК, где 5'-конец происходит от L1, а далее следует экзонная структура соседнего консервативного гена. Так были идентифицированы гоминоид-специфичные изоформы генов, вовлечённых в важные сигнальные пути (например, ELAPOR2, PPP1R1C).
При дифференцировке иПСК в церебральные органоиды (модель раннего развития мозга) (Рис.1(А) общий уровень экспрессии L1 снижался на фоне глобального увеличения метилирования их промоторов. Однако этот процесс оказался неоднородным: значительная часть локусов оставалась деметилированной и высокоактивной, в то время как другие были полностью выключены. Это подчёркивает, что регуляция каждого локуса L1 индивидуальна и зависит от локального геномного контекста.
Подавление L1 в органоидах не изменило спектр формирующихся клеточных типов (нейральные предшественники и нейроны), что указывает на отсутствие влияния на клеточную судьбу. Однако одноядерный РНК-секвенирование выявило значимые транскрипционные сдвиги в популяциях нейральных клеток-предшественников (NPC) Рис.1 (D). В них наблюдалась подавленная экспрессия тех же цис-регулируемых генов, что и в иПСК. Параллельно происходила активация группы генов, ассоциированных с нейрональным ростом, дифференцировкой и синаптогенезом (например, AKAP6, NTRK2). Обогащение этих генов в сигнальных путях указывает на то, что отсутствие L1 смещает баланс в сторону более ускоренного или преждевременного созревания.
Ключевым фенотипическим результатом стало достоверное уменьшение размеров L1-CRISPRi органоидов по сравнению с контролем на этапах активной пролиферации NPC. Это согласуется с транскрипционными данными и свидетельствует о том, что L1 необходимы для оптимальной пролиферации или выживания NPC, возможно, модулируя точный темп их дифференцировки.
Исследование ясно продемонстрировало масштаб цис-регуляторного влияния L1 через функцию альтернативных промоторов. Однако оно не исключает дополнительного вклада транс-регуляторных механизмов, опосредованных L1-РНК или белками, которые могут действовать глобально. Разделение этих двух уровней влияния требует разработки новых молекулярных инструментов.
Включение L1 в регуляторные сети, управляющие нейрогенезом, особенно через гоминоид-специфичные изоформы генов, предполагает их возможный вклад в эволюцию сложного человеческого мозга. Кроме того, обнаруженная связь некоторых L1-регулируемых генов с нейропсихиатрическими расстройствами указывает на то, что полиморфизм по локусам L1 в популяции может влиять на индивидуальную предрасположенность к таким заболеваниям через модуляцию развития мозга.
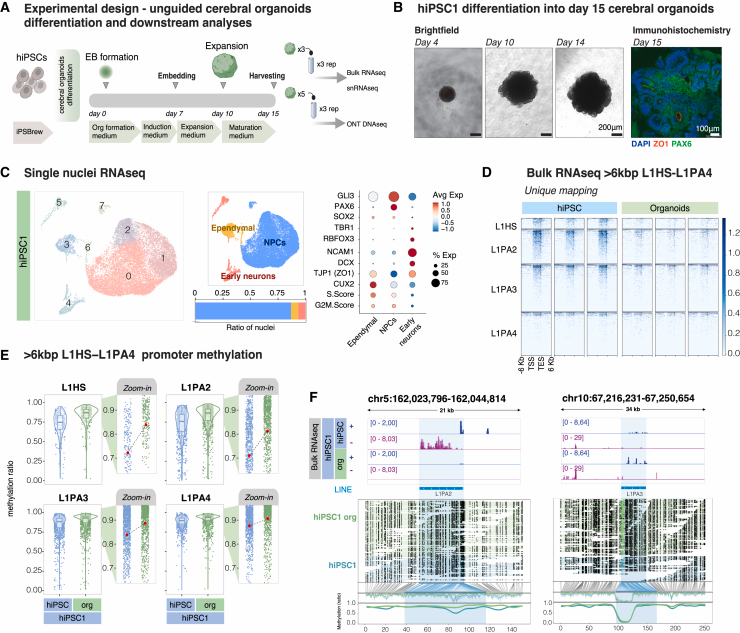
Рис.1 Экспрессия эволюционно молодых полнодлинных L1 в церебральных органоидах. (A) Схема процесса создания неспецифических церебральных органоидов и последующих анализов. (B) Изображения дифференцирующихся церебральных органоидов на разных временных точках и иммуногистохимия органоидов на 15-й день для белков ZO1 (красный) и PAX6 (зеленый). (C) Слева: Проекция показывающая кластеры, обнаруженные в неспецифических церебральных органоидах на 15-й день. В центре, сверху: отображение различных типов клеток, обнаруженных в церебральных органоидах на 15-й день. В центре, снизу: Столбчатая диаграмма, показывающая процентный состав типов клеток в церебральных органоидах на 15-й день дифференцировки. Справа: Точечная диаграмма, отображающая выбранные нейрональные маркеры и маркеры NPC, использованные для характеристики клеточных кластеров (размер точки показывает процент клеток, экспрессирующих ген, цвет указывает на среднюю экспрессию в каждом типе клеток). (D) Экспрессия уникально картированных эволюционно молодых полнодлинных L1 в иПСК человека и церебральных органоидах на 15-й день. (E) Диаграммы, показывающие статус метилирования в промоторной области L1HS-L1PA4 (>6 т.п.н.) в иПСК человека по сравнению с церебральными органоидами на 15-й день. Увеличенные диаграммы показывают средние уровни метилирования (красная точка) для каждого условия и каждого субсемейства. Центры диаграмм соответствуют медиане, границы ящика — первому и третьему квартилю, а усы простираются от квартилей до ±1,5 межквартильного размаха (IQR). (F) Треки в браузере генома, показывающие нормированную транскрипцию L1 (RPKM) в иПСК человека и церебральных органоидах на 15-й день (темно-синий — транскрипция в прямом направлении; фиолетовый — в обратном направлении), длинные риды ДНК ONT для органоидов на 15-й день и иПСК (черные точки указывают на метилированные CpG), и покрытие метилирования элементов L1 внизу (зеленый — органоиды; синий — иПСК человека.
Таким образом, исследование переводит понимание фунуции L1 с уровня «генетического шума» на уровень значимых регуляторных элементов. Оно демонстрирует, что эволюционно молодые L1 представляют собой не однородную массу, а коллекцию индивидуальных геномных модулей, которые интегрированы в транскрипционные сети человеческих плюрипотентных клеток. Их активность добавляет специфичный для приматов слой регуляции, критически важный для координации пролиферации и дифференцировки нейральных предшественников на ранних этапах развития мозга. Полученные данные обосновывают необходимость учёта индивидуальных локусов L1 в будущих исследованиях эволюции человека, нейробиологии развития и этиологии нейрозаболеваний.
Новость подготовила
© с.н.с., к.б.н. Куликова Дина Александровна
12.03.2026