Paternal exercise confers endurance capacity to offspring through sperm microRNAs. Cell Metab. 2025 Nov 4;37(11):2167-2184.e8. doi: 10.1016/j.cmet.2025.09.003..

Область научных интересов: регуляция экспрессии генов, эпигенетика, хроматин, некодирующие РНК.
Идея о наследовании приобретенных признаков лежит в основе эволюционной концепции Ламарка. Хотя она и утратила актуальность с развитием современной эволюционной теории, продолжают накапливаться данные, говорящие о том, что приобретенные признаки могут наследоваться, и такое наследование может быть адаптивным (Liu 2007, Cabej 2021, Sengupta et al. 2023). В основе этих явлений лежат эпигенетические механизмы, которые обусловливают наследуемые изменения экспрессии генов. В последнее время появляется все больше данных, свидетельствующих в пользу того, что носителем эпигенетической информации, передающимся между поколениями, могут быть не только метилирование ДНК или модификации гистонов, но и некодирующие РНК (Cecere 2021). Вклад сперматозоида в цитоплазму зиготы несопоставимо меньше по сравнению с ооцитом, поэтому логично предположить, что наследование цитоплазматических некодирующих РНК реализуется преимущественно по женской линии. Подтверждением этому служит явление гибридного дисгенеза, возникающего при скрещивании дрозофил, несущих разные транспозоны: если транспозоны наследуются от матери вместе с piРНК, направляющими их репрессию, в этом случае потомство развивается нормально, через сперматозоиды же piРНК не передаются, поэтому унаследованные от отцов транспозоны не репрессируются у гибридных потомков, что приводит у них к нарушению развития гонад. В связи с этим особый интерес представляют исследования, показывающие наследование некодирующих РНК от отцов. В работе Yin et al. 2025 установлено, что микроРНК, передающиеся в составе сперматозоидов, служат ключевым звеном механизма эпигенетического наследования приобретенной физической выносливости.
Регулярные физические тренировки оказывают комплексное воздействие на организм, особенно на состояние опорно-двигательной системы, причем характер изменений определяется характером нагрузок: кратковременные силовые тренировки в большей степени увеличивают мышечную массу и силу, в то время как более продолжительные аэробные нагрузки – выносливость, что позволяет адаптироваться к регулярно возникающему типу нагрузки. Адаптация проявляется в изменении не только структуры, но и метаболизма мышечных волокон: кратковременные интенсивные нагрузки могут быть обеспечены энергией, получаемой в результате быстрых процессов анаэробного гликолитического расщепления глюкозы, в то время как длительные нагрузки меньшей интенсивности требуют более медленного, но эффективного процесса окислительного фосфорилирования, протекающего в митохондриях (Smith et al. 2023).
Авторы обсуждаемой работы показали, что регулярные тренировки мышей на беговой дорожке приводят к увеличению мышечной массы и физической выносливости (времени, которое мыши могут находиться под нагрузкой до изнеможения) по сравнению с контролем (мыши, ведущие обычный образ жизни без дополнительных нагрузок). Кроме того, тренированные мыши демонстрировали повышенное потребление кислорода и пониженное содержание молочной кислоты в крови после нагрузки, что указывало на активизацию окислительного метаболизма. Дальнейшие исследования показали увеличение пропорции окислительных мышечных волокон по сравнению с гликолитическими. Для окислительных волокон характерно увеличенное содержание митохондрий и повышенная активность ферментов, обеспечивающих окислительное фосфорилирование.
Было показано, что приобретенные в результате тренировок характеристики передаются потомкам: без специальных тренировок у них наблюдалась повышенная выносливость, увеличенная пропорция окислительных мышечных волокон, более высокое содержание митохондрий и повышенная активность ряда дыхательных ферментов, в частности, сукцинатдегидрогеназы (ключевого компонента одновременно цикла трикарбоновых кислот и митохондриальной электрон-транспортной цепи), по сравнению с потомством контрольных нетренированных мышей. Кроме того, мышцы у потомков тренированных мышей демонстрировали повышенное содержание гликогена и более интенсивное потребление глюкозы, судя по данным позитронной эмиссионной томографии, позволяющей отслеживать накопление в клетках радиоактивно меченого аналога глюкозы. Также наблюдалась повышенная экспрессия белка GLUT4, осуществляющего перенос глюкозы в клетки. Следующим поколениям эти изменения не передавались: внуки тренированных мышей не отличались от контрольных.
Какие молекулярные механизмы запускают наблюдаемые изменения? Среди генов, экспрессия которых была повышена как у тренированных мышей, так и у их потомства, особое внимание исследователей привлек ген PGC-1α (peroxisome proliferator-activated receptor gamma coactivator 1-alpha), являющийся мастер-регулятором биогенеза митохондрий (Qian et al. 2024). Чтобы выяснить, не является ли повышение экспрессии этого гена ключевым триггером изучаемых изменений, была использована трансгенная конструкция, обеспечивающая дополнительную экспрессию PGC-1α в мышечной ткани. Было показано, что такая сверхэкспрессия сама по себе безо всяких тренировок достаточна для повышения выносливости и сопутствующих структурных и биохимических изменений в мышечных волокнах. Особый интерес представляют результаты скрещивания мышей, несущих одну копию трансгена PGC-1α, с мышами дикого типа. В потомстве такого скрещивания были как особи, унаследовавшие трансген, так и особи без трансгена. Изменения, ассоциированные с увеличением выносливости, наблюдались не только у трансгенного потомства, но и у мышей, чьи отцы несли трансген, но сами они его не унаследовали. Это говорит о том, что повышение экспрессии PGC-1α в родительском организме способно запустить эпигенетически наследуемые изменения.
За счет каких механизмов обеспечивается передача изучаемых изменений потомству? Могут ли в качестве носителя эпигенетической информации выступать молекулы РНК? Чтобы ответить на эти вопросы, авторы работы получили препараты тотальной РНК из сперматозоидов тренированных и нетренированных мышей и инъецировали их в зиготы с последующей имплантацией суррогатным матерям и развитием во взрослых особей. Мыши, полученные из зигот с инъекцией РНК из сперматозоидов тренированных самцов, демонстрировали повышенную мышечную массу и выносливость, а также комплекс сопутствующих морфологических и биохимических изменений в мышечных волокнах по сравнению с тем, что наблюдалось в случае инъекции РНК от нетренированных самцов. Эти результаты говорят о том, что РНК несет информацию, достаточную для запуска развития изучаемых изменений. Но какие компоненты тотальной РНК существенны в данном случае? Чтобы ответить на этот вопрос, были изолированы отдельные фракции длинных и коротких РНК (больше или меньше 200 нуклеотидов соответственно). Аналогичные вышеописанным эксперименты с микроинъекцией этих фракций в зиготы показали, что за формирование изучаемых изменений отвечает фракция коротких РНК.
Чтобы выяснить, как тренировки влияют на содержание коротких РНК в сперматозоидах, с использованием метода глубокого секвенирования были проанализированы профили коротких РНК из сперматозоидов тренированных, нетренированных, а также несущих трансген PGC-1α мышей. Существенные изменения были показаны для микроРНК. Последующая валидация данных при помощи количественного ОТ-ПЦР-анализа подтвердила достоверное увеличение содержания 10 микроРНК в сперматозоидах тренированных и трансгенных самцов по сравнению с нетренированными. Кроме того, были проанализированы обусловленные тренировками изменения содержания микроРНК в сперматозоидах людей. 7 из 10 микроРНК оказались консервативными и активировались в результате тренировок, что говорит в пользу возможной универсальности изучаемых механизмов.
Но действительно ли микроРНК из сперматозоидов попадают в ооцит в результате естественного оплодотворения? Для прояснения этого вопроса были проанализированы профили коротких РНК в зиготах на стадии двух пронуклеусов, до активации транскрипции собственного генома. Была показана ожидаемая разница в количествах изучаемых микроРНК в зиготах, полученных в результате естественного оплодотворения ооцитов сперматозоидами от тренированных и нетренированных самцов.
Какие гены регулируются установленными микроРНК? Предсказание генов-мишеней микроРНК, содержание которых в сперматозоидах увеличивалось вследствие тренировок, и последующий Gene Ontology анализ позволили построить регуляторную сеть, центральными элементами которой были гены MED13, NSD1 и NCoR1, они регулировались наибольшим количеством изучаемых микроРНК. Эти гены кодируют регуляторы транскрипции. Особое внимание авторы уделили NCoR1, поскольку уже имелись данные о его роли в адаптации мышц к нагрузке (Yamamoto et al. 2011). NCoR1 – это транскрипционный корепрессор, который рекрутирует деацетилазы гистонов, препятствуя тем самым функциям ряда транскрипционных факторов, запускающих процессы увеличения мышечной массы и образования новых митохондрий. Интересно отметить, что эти транскрипционные факторы активируются при участии PGC-1α, то есть PGC-1α и NCoR1 – функциональные антагонисты. Таким образом, вырисовывается молекулярный механизм влияния унаследованных микроРНК: они репрессируют NCoR1, а это, в свою очередь, обусловливает изменения в мышцах развивающегося эмбриона.
Чтобы выяснить, влияют ли наследуемые через сперматозоиды микроРНК на экспрессию гена NCoR1, авторы работы сначала при помощи репортерной люциферазной системы подтвердили, что кандидатные микроРНК действительно связываются с 3’-нетранслируемой областью мРНК NCoR1, а потом при помощи иммуноокрашивания и конфокальной микроскопии показали, что количество белка NCoR1 меньше в эмбрионах, получивших микроРНК из сперматозоидов тренированных мышей. Микроинъекция искусственно синтезированной микроРНК miR-148a-3p в нормальные зиготы приводила к уменьшению содержания NCoR1 в клетках развивающихся эмбрионов. Сформировавшиеся из таких эмбрионов взрослые мыши обладали большей мышечной массой, повышенной физической выносливостью и соответствующим комплексом морфологических и биохимических изменений в мышечных волокнах по сравнению с контролем (инъекция коротких РНК, не имеющих мишеней среди мРНК мыши). То есть даже одна из изучаемых в работе микроРНК способна запустить процессы, приводящие к комплексу изменений.
Действительно ли именно обусловленная микроРНК репрессия гена NCoR1, а не какие-то дополнительные неучтенные механизмы, является причиной изучаемых изменений в мышцах? Чтобы ответить на этот вопрос, был проведен эксперимент со «спасением» (rescue) фенотипа. Суть его в следующем: в зиготы, получившие микроРНК из сперматозоидов тренированных мышей, была инъецирована плазмида, экспрессирующая NCoR1 на достаточно высоком уровне, чтобы преодолеть эффекты микроРНК. Мыши, сформировавшиеся из таких зигот, обладали сниженной выносливостью и содержанием митохондрий в мышечных волокнах по сравнению с контролем (инъекция контрольной плазмиды). Это говорит о том, что наблюдаемые эффекты действительно обусловлены регуляцией экспрессии NCoR1.
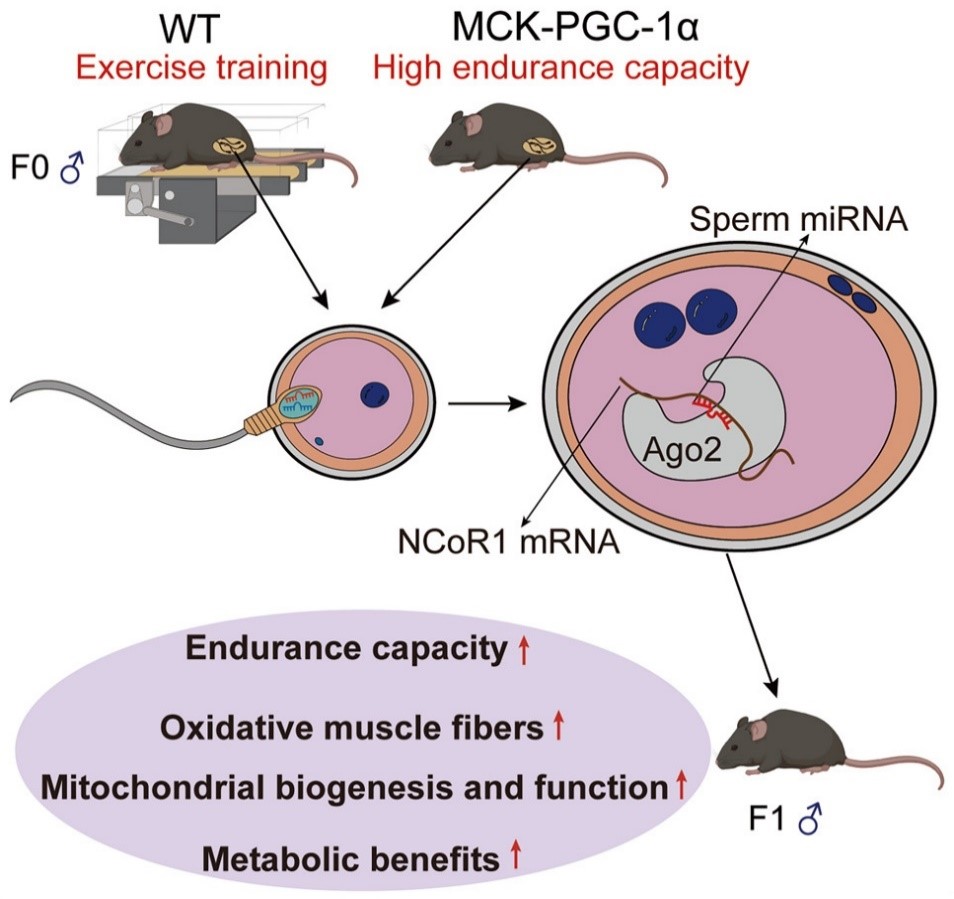
Проведенные исследования позволяют предложить следующую модель (Рис. 1): физические тренировки запускают в мышцах адаптивные процессы, ключевым механизмом которых является активация гена PGC-1α, который, в свою очередь, запускает генетическую программу, обеспечивающую усиление биогенеза митохондрий и активизацию окислительного метаболизма в мышечных волокнах. Кроме того, результатом работы этих механизмов является изменение спектра микроРНК, включаемых в состав сперматозоидов, в частности, увеличивается содержание микроРНК к гену транскрипционного репрессора NCoR1, функционального антагониста PGC-1α. В результате оплодотворения эти микроРНК попадают в зиготу, обеспечивая репрессию гена NCoR1, что, в свою очередь, запускает в формирующемся эмбрионе комплекс молекулярных, биохимических и структурных изменений в мышечных волокнах, аналогичных тем, что происходили в родительском организме в результате тренировок.
Рис. 1. Общая схема механизма наследования физической выносливости при участии микроРНК. Иллюстрация из обсуждаемой статьи.
Остается открытым вопрос о механизме влияния тренировок на состав микроРНК в сперматозоидах. Авторы предполагают возможную роль внеклеточных везикул, которые через кровоток могли бы доставлять микроРНК из мышечной ткани в гонады. Альтернативное объяснение подразумевает роль обусловленных тренировками гормональных изменений в организме, которые могли бы повлиять на экспрессию микроРНК в гонадах. Еще один важный вопрос касается механизмов влияния репрессии NCoR1 в зиготе на дальнейшее развитие зародыша. Работа каких генетических программ изменяется при репрессии этого гена? Почему итоговые изменения затрагивают именно мышечные клетки, но при этом неодинаковы в разных мышцах? В каких еще органах и тканях могут наблюдаться схожие механизмы наследования приобретенных признаков?
В конце хотелось бы коснуться вопроса о значении подобных механизмов наследования приобретенных признаков. Очевидно, что их открытие не ставит под вопрос классический механизм эволюции, основанный на ненаправленных генетических изменениях и естественном отборе, но расширяет представления о процессах адаптации к изменяющимся условиям. Эпигенетическое наследование подразумевает запуск готовых генетических программ, а потому позволяет гибко, оперативно и достаточно предсказуемо реагировать на изменения, с которыми организм сталкивался в своем эволюционном прошлом. Например, регулярное увеличение физической активности может подразумевать появление каких-то новых факторов, которых необходимо активно избегать (таких, как хищники), возникшие трудности с добыванием пищи, требующие дополнительных усилий, либо неблагоприятные изменения условий среды, стимулирующие миграцию. В данных случаях преадаптация потомства к новым условиям будет полезна. Если же условия со временем вернутся к норме, эпигенетические механизмы столь же оперативно обратят физиологические изменения вспять, что было бы затруднительно для классического эволюционного механизма с отбором мутаций или вариантов генов.
Список литературы
- Cabej N.R. A mechanism of inheritance of acquired traits in animals. Dev Biol. 2021 Jul:475:106-117. doi: 10.1016/j.ydbio.2021.03.004.
- Cecere G. Small RNAs in epigenetic inheritance: from mechanisms to trait transmission. FEBS Lett. 2021 Oct 29;595(24):2953–2977. doi: 10.1002/1873-3468.14210.
- Liu Y. Like father like son. A fresh review of the inheritance of acquired characteristics. EMBO Rep. 2007 Sep;8(9):798–803. doi: 10.1038/sj.embor.7401060
- Qian L., Zhu Y., Deng C., Liang Z., Chen J., Chen Y., Wang X., Liu Y., Tian Y., Yang Y. Peroxisome proliferator-activated receptor gamma coactivator-1 (PGC-1) family in physiological and pathophysiological process and diseases. Signal Transduct Target Ther. 2024 Mar 1;9(1):50. doi: 10.1038/s41392-024-01756-w.
- Sengupta T., Kaletsky R., Murphy C.T. The Logic of Transgenerational Inheritance: Timescales of Adaptation. Annu Rev Cell Dev Biol. 2023 Oct 16:39:45-65. doi: 10.1146/annurev-cellbio-020923-114620.
- Smith J.A.B., Murach K.A., Dyar K.A., Zierath J.R. Exercise metabolism and adaptation in skeletal muscle. Nat Rev Mol Cell Biol. 2023 Sep;24(9):607-632. doi: 10.1038/s41580-023-00606-x.
- Yamamoto H., Williams E.G., Mouchiroud L., Cantó C., Fan W., Downes M., Héligon C., Barish G.D., Desvergne B., Evans R.M., Schoonjans K., Auwerx J. NCoR1 is a conserved physiological modulator of muscle mass and oxidative function. Cell. 2011 Nov 11;147(4):827-39. doi: 10.1016/j.cell.2011.10.017.
Новость подготовил
© Шацких Алексей Сергеевич, к.б.н., старший научный сотрудник лаборатории функциональной геномики.
11.12.2025