Design of highly functional genome editors by modelling CRISPR-Cas sequences.
Nature. 2025 Sep;645(8080):518-525.
doi: 10.1038/s41586-025-09298-z.

Научные интересы: генетика пола, эпигенетическая регуляция активности генов,
генетика развития, гаметогенез, piРНК-сайленсинг, межвидовые гибриды,
гибридный дисгенез, эволюционная генетика
В последние годы технология редактирования генома стала одним из ключевых элементов во множестве отраслей естественных наук, биотехнологии, медицине и сельском хозяйстве. Среди различных методов редактирования генома CRISPR–Cas системы заняли центральное место благодаря своей точности и простоте использования. Несмотря на это, применение таких систем часто сталкивается с функциональными ограничениями. Несмотря на то, что было разработано большое количество новых систем на основе CRISPR-Cas для различных бактериальных и вирусных геномов, они зачастую демонстрируют проблемы с базальной активностью в клетках-мишенях, температурным оптимумом и другими показателями. Однако, в своей работе, вышедшей в июле 2025 года в журнале Nature, Джеффри Руффало и его коллеги из США и Швейцарии представили инновационный подход, основанный на использовании искусственного интеллекта для преодоления ограничений работы CRISPR-Cas системы и разработки высокоэффективных редакторов генома.
Основой для исследования стала разработка и использование языковых моделей, которые обучались на большой выборке разнообразных белковых последовательностей. Эти модели помогают воспроизвести структуры и функции белков, не прибегая к сложным структурным гипотезам, которые часто являются узким местом в традиционных методах белкового дизайна. Конечная цель заключалась в создании серии новых CRISPR–Cas белков, существенно отличающихся от известных природных аналогов, но обладающих улучшенными функциональными характеристиками.
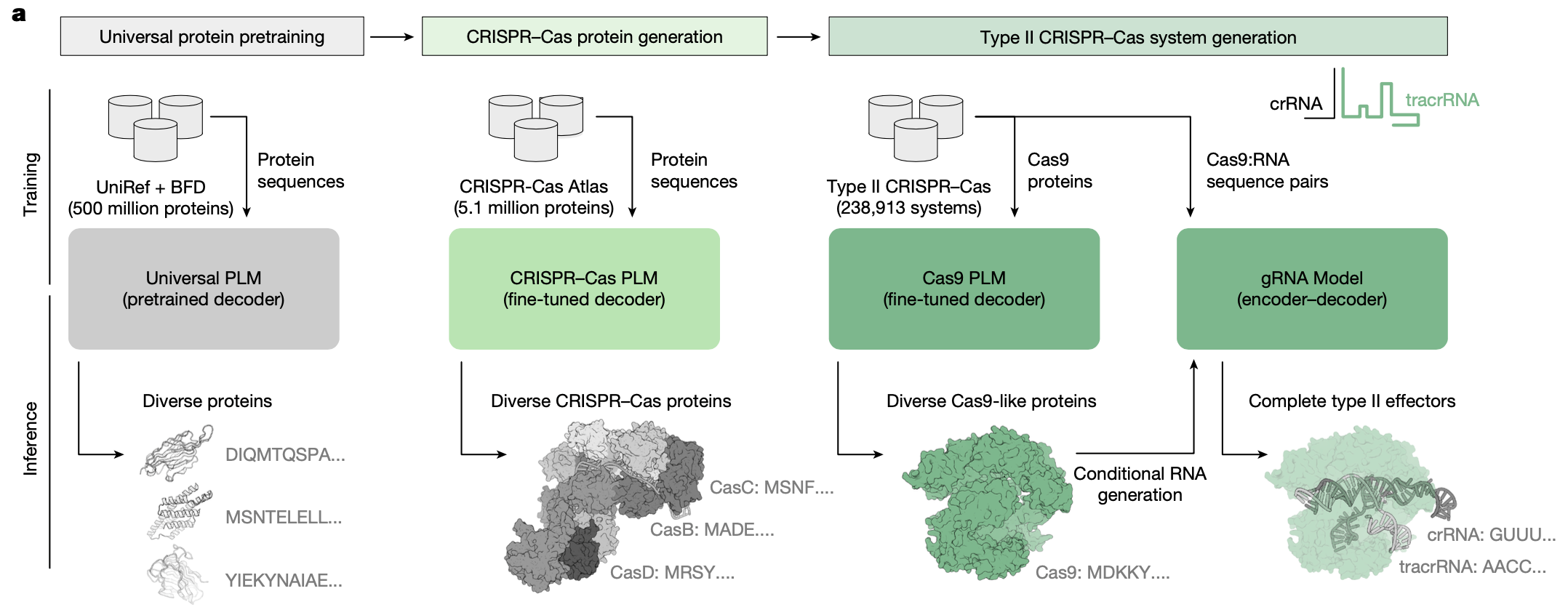
В основе исследования лежало использование языковых моделей белков (Language models – LMs), основанных на коэволюционном плане строения белка, лежащем в основе его функции. Д. Руффало и коллеги создали массив данных, содержащий свыше одного миллиона CRISPR оперонов, извлечённых путем систематического анализа 26 терабаз геномных и метагеномных данных. Это позволило значительно расширить естественное разнообразие CRISPR–Cas-систем, доступных для моделирования и потенциального использования в прикладных задачах (рис. 1).
Рис. 1. Обзор подхода к языковому моделированию для проектирования систем CRISPR–Cas. LM изучают общие ограничения эволюции белков посредством предварительной подготовки на различных белках, охватывающих эволюционное дерево, а затем специализируются на проектировании путем тонкой настройки на данных о белках Cas и нуклеиновых кислотах
Важным аспектом исследования также является демонстрация способности языковых моделей генерировать уникальные белки, которые значительно выходят за пределы видимого естественного разнообразия. Так, Д. Руффало с коллегами удалось создать в 4,8 раз больше белковых кластеров, чем обнаружено в природе. Такие результаты, безусловно, открывают новые возможности для биоинженерии.
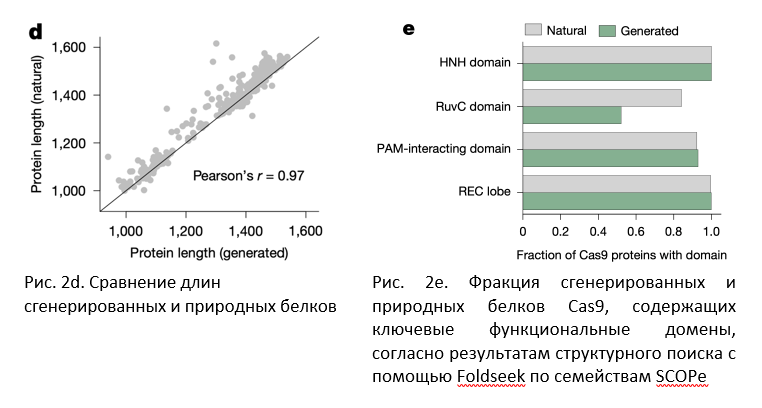
Для оценки «жизнеспособности» сгенерированных белков исследователи сравнивали длины полученных и природных последовательностей. В целом, сгенерированные последовательности соответствовали длине природных белков из того же кластера. Также, чтобы оценить структуру сгенерированных Cas9-подобных белков, авторы использовали AlphaFold2 для прогнозирования структур 5000 сгенерированных и 5000 природных последовательностей, анализ показал значительное совпадение. Помимо этого, Д. Руффало и соавторы подтвердили наличие большинства основных доменов Cas9 в большинстве полученных белков (рис. 2).
Известно, что для работы таких систем редактирования генома важен ещё один молекулярный компонент – гидовая РНК (gRNA), которая, в свою очередь, состоит из последовательности целевой РНК (спейсера), повтора CRISPR-РНК (crRNA) и tracrRNA, при этом tracrRNA и crRNA обычно получают из природных систем. В качестве первоначальной проверки модели gRNA исследователи разработали десять gRNA для набора эффекторных белков, ранее использовавшихся в качестве редакторов генома. Каждая из разработанных gRNA, а также природные gRNA, полученные в результате анализа метагенома, были отформатированы в однонаправленные РНК (sgRNA). Исследователями было обнаружено, что разработанные на основе модели sgRNA были аналогичны природным sgRNA для каждого белка. В качестве дополнительной проверки было обнаружено, что пары crRNA:tracrRNA часто образуют канонический дуплекс и что модель может точно предсказать совместимость sgRNA между различными ортологами Cas9. Таким образом, данная модель может быть эффективно использована для создания функциональных sgRNA для сгенерированных Cas9-подобных белков.
Одним из ключевых достижений работы стал редактор генов, названный самими исследователями OpenCRISPR-1. OpenCRISPR-1 продемонстрировал уровни активности, сопоставимые с SpCas9 (Cas9 Streptococcus pyogenes) в целевых участках, при этом на 95% сократилось количество правок на известных нецелевых (off-target) участках для SpCas9. Помимо этих впечатляющих показателей, исследователями было убедительно показано, что OpenCRISPR-1 является менее иммуногенным для человеческого организма по сравнению с SpCas9, что особенно важно при использовании в терапевтических целях.
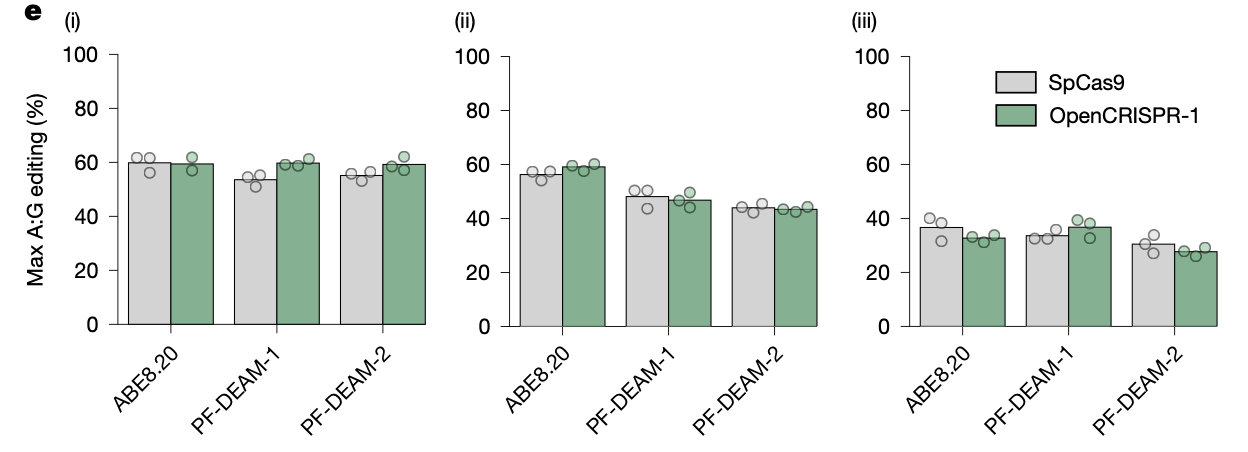
Также OpenCRISPR-1 показал хорошие результаты при использовании в качестве однонуклеотидного редактирования генома без внесения двуцепочечных разрывов в ДНК. Для исследования таких возможностей данного белка Д. Руффало и его коллеги преобразовали OpenCRISPR-1 в никазу и совместили её с ранее сконструированной аденозиндезаминазой (ABE8.20), обычно используемой при редактировании азотистых оснований. Исследователи наблюдали устойчивую замену A-G с помощью редактора оснований OpenCRISPR-1 на всех трёх целевых сайтах (показатель редактирования 35–60%), что было сопоставимо с системой редактирования оснований ABE8.20, использующей никазу SpCas9 (рис. 3)
Рис. 3. Сравнение эффективности замен А-G двух систем редактирования: на основе SpCas9 и OpenCRISPR-1
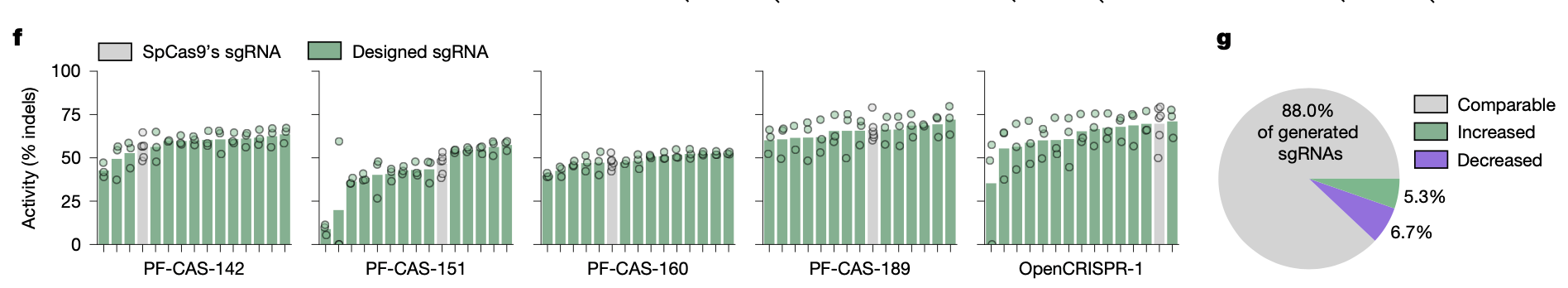
На следующем этапе работы Д. Руффало с коллегами, используя описанную ранее модель генерации gRNA, сконструировали 14 sgRNA для каждого из 5 сгенерированных Cas9-подобных белков (включая OpenCRISPR-1), и протестировали редактирования в клетках HEK293T в целевом участке HEK3. В большинстве случаев исследователи наблюдали улучшенное редактирование с 31 дизайнированными sgRNA по сравнению с sgRNA SpCas9, включая значительные улучшения редактирования для четырёх sgRNA для двух из пяти вариантов (рис. 4).
Рис. 4 f. Эффективность редактирования в целевом сайте HEK3 с помощью разработанных sgRNA (зелёный) и sgRNA SpCas9 (серый). Четыре из пяти полученных белков продемонстрировали повышенную эффективность редактирования с помощью разработанных sgRNA; 4 g. Изменение эффективности редактирования по сравнению с sgRNA SpCas9. Большинство разработанных sgRNA демонстрируют эффективность, которая достоверно не отличается от рекомендуемой SpCas9, тогда как определённая подгруппа либо значительно улучшает, либо ухудшает эффективность редактирования (t-критерий P < 0,05)
Важно отметить, что OpenCRISPR-1, показавший стабильно высокую эффективность редактирования в предыдущих экспериментах, показал схожие результаты с разработанной sgRNA или sgRNA SpCas9. Это указывает на то, что OpenCRISPR-1 может быть применим либо как часть полностью сгенерированного редактора генов, либо как заменитель SpCas9 в существующих системах редактирования.
Несмотря на значительные достижения, описанные в работе, исследователи признают необходимость дальнейших исследований для полного понимания и реализации потенциала, который предлагают синтетические редакторы OpenCRISPR. В будущем останется важным исследовать их эффективность и устойчивость в различных экспериментальных условиях и клеточных типах. Кроме непосредственного редактора OpenCRISPR-1, представленный в работе подход может быть применен к другим классам систем CRISPR, расширяя их потенциальные применения. Научное сообщество может в дальнейшем рассмотреть возможность использования таких инструментов для разработки редакторов, специально адаптированных для определённых нужд, как в медицинской практике, так и в сельском хозяйстве.
Работа Д. Руффало и его коллег подтверждает важность и эффективность интеграции технологий искусственного интеллекта в биологические исследования и разработки. Использование языковых моделей для проектирования белков открывает двери для создания уникальных геномных редакторов, которые способны решать текущие вызовы и предлагать инновационные решения в медицине и науке. Исследователи сделали важнейший шаг к трансформации CRISPR технологий, делая их более доступными и пригодными для решения широкого спектра задач.
Новость подготовил
© кандидат биологических наук, младший научный сотрудник Адашев Владимир Евгеньевич
07.11.2025