«The divergent intron-containing actin in sponge morphogenetic processes»,
опубликованной в журнале NAR Genomics and Proteomics Jun 4;7(2):lqaf071.
doi: 10.1093/nargab/lqaf071. eCollection 2025 Jun.

Научные интересы: протеасомные механизмы развития ЦНС и нейродегенеративных заболеваний.

Научные интересы: молекулярная генетика дрозофилы.
Возникновение многоклеточности тесно связано с эволюцией механизмов адгезии и взаимодействия между клетками. Способность клеток к объединению является ключевой на ранних этапах эмбрионального развития и регенерации у животных. У большинства животных формирование in vivo нового целостного организма из суспензии диссоциированных клеток не происходит, однако некоторые виды реализуют это удивительное свойство. Особенно примечательны в этом отношении губки (тип Porifera), способные к созданию новой особи после диссоциации тела на отдельные клетки [1]. Во время самосборки клеточных агрегатов клетки губок активно двигаются и претерпевают многочисленные трансформации. Помимо губок, способность к полной или частичной регенерации демонстрируют такие организмы, как гидры, планарии и асцидии, а также эмбриональные клетки рыб, земноводных и пресмыкающихся. У млекопитающих процессы самосборки и реагрегации клеток лежат в основе технологий выращивания органоидов in vitro. Одним из ключевых белков в реализации этих процессов является белок цитоскелета – актин, участвующий в подвижности клеток, адгезии, поляризации и сигнализации. Известно, что актин может находиться в двух формах: мономерной (G-актин) и филаментной (F-актин), а его динамика контролируется рядом факторов, включая уровень АТФ, различные ионы и специфические актин-связывающие белки. Считается, что в структуре генов актина существует скрытый код, который контролирует функциональное разнообразие изоформ актина [2]. Эукариотические актины имеют очень похожие аминокислотные последовательности и различаются на уровне нуклеотидов, особенно в их экзонно-интронной организации. Гетерологичные изоформы актина позволяют цитоскелету динамично реагировать на внешние воздействия, сохраняя жизнеспособность клеток. Экспрессия изоформ актина на уровне белка у млекопитающих тканеспецифична. Немышечные клетки млекопитающих экспрессируют β- и γ-актин, которые практически идентичны (99%), но локализованы в разных клеточных компартментах. Нарушение экспрессии гена β-актина вызывает эмбриональную гибель у мышей, тогда как нарушения экспрессии γ-актина не являются летальными [3].
Какие особенности актинового цитоскелета позволяют губкам переживать диссоциацию их тела на отдельные клетки и образовывать клеточные агрегаты для восстановления нового организма? Какие изоформы актина существуют у губок и какие функции они выполняют в процессе реагрегации? Выявлению особенностей актина у губок в реализации их пластичности посвящена данная статья.
Коллектив российских ученых из Института биологии развития им. Н.К. Кольцова РАН, НИИ Физико-химической биологии имени А. Н. Белозерского МГУ, Сколковского Института науки и технологий и Казанского Федерального Университета провели уникальное масштабное исследование роли ключевого белка цитоскелета - актина в процессах регенерации и морфогенеза у одной из древнейших из ныне существующей группы многоклеточных животных – губок (тип Porifera). Объектом исследования стала морская холодноводная губка Halisarca dujardinii, обладающая высокой скоростью восстановления нового целостностого организма из механически диссоциированных клеток. Исследование объединило глубокий молекулярно-биологический анализ на основе секвенирования РНК единичных клеток (scRNA-seq), секвенирования мРНК диссоциированных клеток и клеточных агрегатов губок, собранных в разные периоды репродуктивного цикла (bulk RNA-seq), FISH гибридизации, протеомного анализа и посттрансляционных модификаций белков (LC-MS/MS) и иммунофлуоресцентную и электронную микроскопию. Впервые такие комплексные подходы были применены к изучению роли актина и его динамики в регенеративных механизмах у базальных животных.
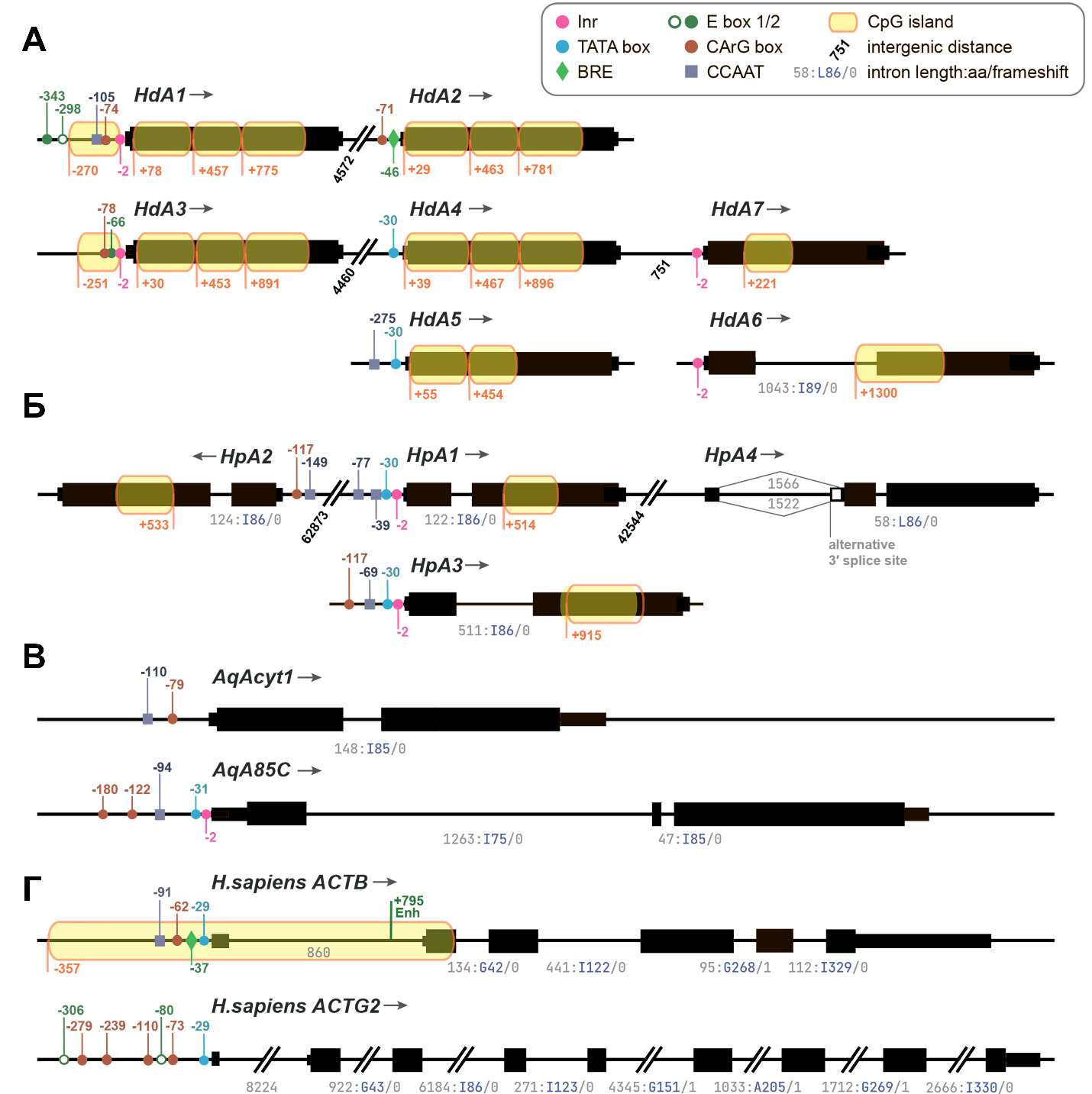
У губок, в том числе и у губки H. dujardinii, авторы обнаружили неожиданное разнообразие генов актина (Рис.1). HdA1, HdA2, HdA3, HdA4, HdA5, HdA7 губки H. dujardinii – консервативные гены актина без интронов, а HdA6 - функционально дивергентный, содержащий интрон ген актина (Рис. 1). Актины различаются не только по экзонно-интронной структуре, но и по регуляторным областям (Рис.1), предполагая различия в их экспрессии. Гены HdA1, HdA2, HdA3 характеризутся высоким уровнем экспрессии, в то время как уровень экспрессии дивергентного актина HdA6 на порядок ниже (Рис. 3Б). Сравнительный анализ положения интронов в генах актина показал, что интроны в позиции I85 консервативны у большинства животных и человека [4]. У гребневиков интрон в позициии I85 отсутствует, но есть другие – в позициях: G15, G168 и M356. Очевидно, актины гребневиков представляет собой предковые формы генов актина. У представителей разных классов губок: H. dujardinii (кл. Demospongiae) и Oscarella minuta (кл. Hexactinellida) только один ген актина содержит интрон, остальные актины без интронов, и, вероятно, возникли в результате генных дупликаций или ретротранспозиций.
Рис. 1. Регуляторные элементы генов актина у губок и человека. (A) H. dijardinii; (Б) H. panicea; (В) A. queenslandica консервативный (AqAcyt1) и неконсервативный актин (AqA85C); (Г) человеческий β- (ACTB) и γ-актин (ACTG2). На рисунке показаны мотивы ДНК, участвующие в регуляции генов, включая элементы основного промотора (TATA-бокс, инициатор (Inr) и элемент распознавания фактора транскрипции B (BRE)). Кроме того, присутствуют CpG-острова, которые могут быть связаны с экспрессией генов «домашнего хозяйства». Указаны последовательности ДНК, участвующие в регуляции генов актина у билатеральных животных: E-box1, E-box2, CCAAT-box, CArG-box. Энхансер ATGGTAATAA, расположенный в интроне генов актина позвоночных, показан для человеческого гена, но не обнаружен у губок. Координаты элементов указаны относительно точек начала транскрипции соответствующих генов. Старт начала транскрипции HdA1, HdA2 и HdA3 H. dujardinii была определена с помощью RACE. Для других генов актина начало транскрипции было предсказано на основе транскриптомных данных. Альтернативный 3′-сайт сплайсинга обнаружен в гене HpA4 (B). Стрелки обозначают направление транскрипции; чёрные цифры – расстояние между генами актина, расположенными на одном скаффолде; оранжевые цифры – начало CpG-островов; серые цифры – длина интронов.
Несмотря на наличие 7 генов актина у губки H. dujardinii протеомными методами исследования были выявлены только HdA1/2/3 и HdA6 белковые продукты. Актин HdA6 присутствует в ядрах и цитоплазме клеток, тогда как HdA1/2/3 только в цитоплазме. Определены посттрансляционные модификации актинов и их сайтов взаимодействия с актин-связывающими белками. Масс-спектрометрия (LC-MS/MS) выявила значительные различия между посттрансляционными модификациями актинанов: HdA1/2/3 подвергается ацетилированию, метилированию, окислению метионина и убиквитинированию, что влияет на его стабильность и функциональную активность. Окисление метионина в позициях M16, M44, M47 и M305 свидетельствует о чрезвычайно высокой чувствительности этих актинов к уровню реактивных форм кислорода (ROS), сигнальных молекул, связанных с клеточной адаптацией. Кроме того, было установлено, что актины HdA1/2/3 и HdA6 связываются с ферритином [5]. Это позволило предположить, что актиновый цитоскелет через редокс-сигналы участвует в гем-зависимых реакциях, особенно в условиях механического стресса и регенерации. Распределение актина в клетках губок различно (Рис.2) и зависит от редокс-статуса. Клетки губок имели разную чувствительность к действию ингибитора деполимеризации актина, жасплакинолида. Так, звездчатые и амёбоидные клетки демонстрировали стабилизацию F-актина при высоком уровне ROS. Это говорит о том, что окислительные стресс играет регуляторную роль в изменении структуры актинового цитоскелета у губок. С помощью ингибитора деполимеризации актина, жасплакинолида, установлено, что динамика актина критически важна для структурной перестройки клеток при формировании клеточных агрегатов и сохранения их потенциала восстановления нового целостного организма. Это позволило не только описать клеточное разнообразие у губки H. dujardinii, но и понять, как разные формы актина участвуют в морфогенезе, адаптации к механическому стрессу и регенерации.
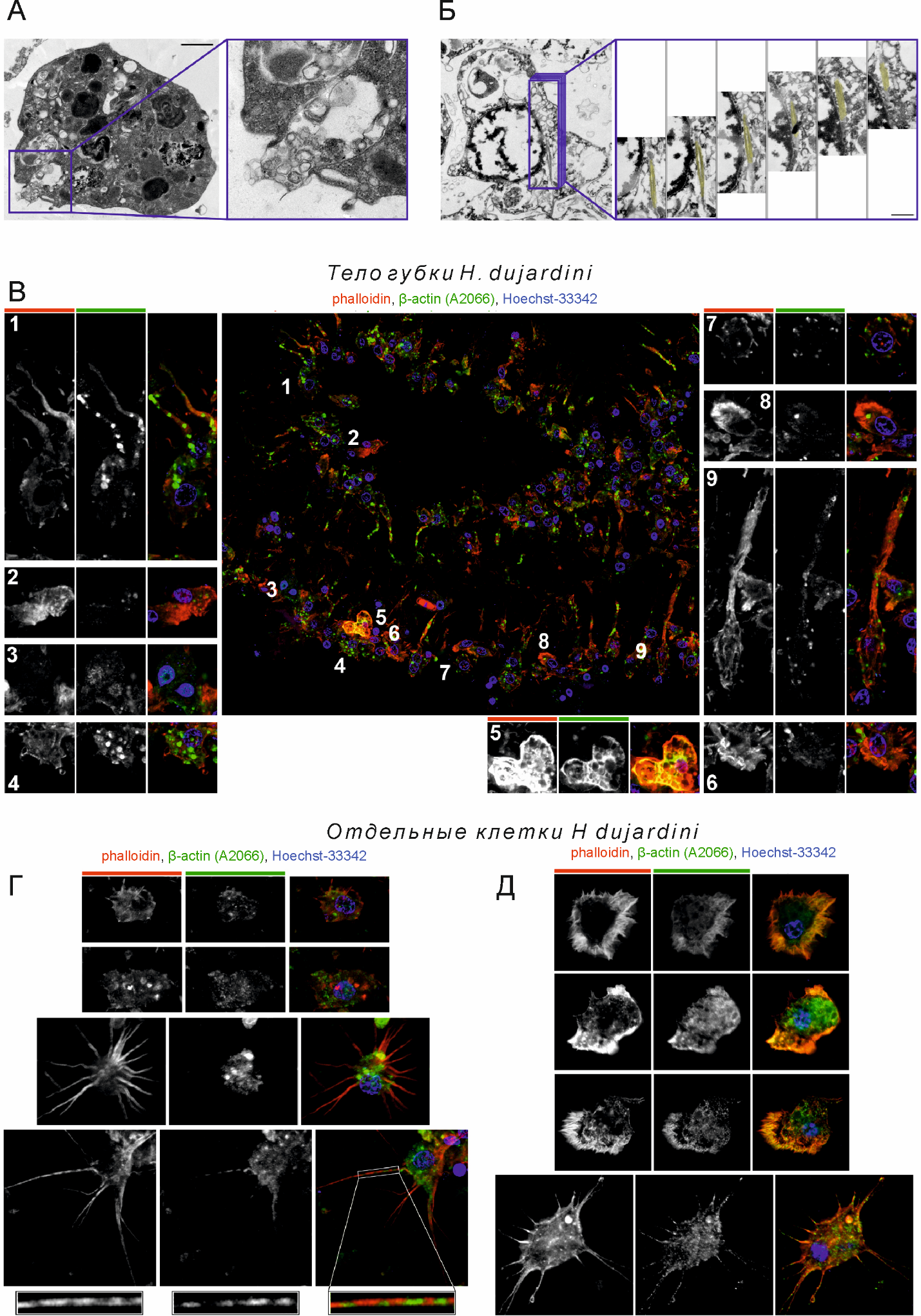
Рис. 1. Распределение актиновых структур в теле губки H. dujardinii и ее диссоциированных клетках.
(А) Эндо-/экзоцитоз, зафиксированные с помощью ТЭМ (трансмиссионной электронной микроскопии), демонстрирует активные актин-зависимые процессы в клетках губки. Выделенная область показана при увеличении справа. Шкала: 1 мкм.
(Б) Изображение ТЭМ, демонстрирующее плотный пучок актиновых микрофиламентов в цитоплазме клетки губки (выделен жёлтым псевдоцветом). Последовательные ультратонкие срезы из области, обведённой кружком, показаны справа увеличенными. Шкала: 500 нм.
(В) Флуоресцентные изображения, демонстрирующие распределение актина в теле губки H. dujardinii. Окрашивание фибриллярного (полимеризованного) актина фаллоидином (красный), антителами к β-актину A2066 (зелёный), ядра окрашены Hoechst 33342 (синий). У клеток без выростов наблюдаются выраженные стрессовые филаменты различных размеров (2), ламеллы (6), диффузное распределение актина в цитоплазме (3), крупные или мелкие актиновые гранулы в цитоплазме (4, 7, 8), или многочисленные актиновые пучки и поперечные дуги (5). В клетках с выростами актиновые гранулы разных размеров наблюдаются как в соме клетки, так и в выростах; окрашивание фаллоидином более выражено в выростах (1, 9).
(Г) Окрашивание диссоциированных клеток губки фаллоидином (красный), антителами к β-актину A2066 (зелёный) и Hoechst 33342 (синий). Сверху вниз: неполяризованная неподвижная клетка с актиновыми гранулами, окрашенными либо только антителами, либо только фаллоидином; в клетках с выростами окрашивание фаллоидином преобладает в выростах (как в C), а антитела к β-актину выявляют гранулы в соме клетки (третья сверху) или как в соме, так и в выростах (нижняя панель). В последнем случае окрашивание фаллоидином, по-видимому, исчезает в областях, где присутствует окрашивание антителами, без колокализации (обведено и увеличено ниже).
(Д) Окрашивание диссоциированных клеток губки фаллоидином (красный), антителами к β-актину ACTB 11B7 (зелёный) и Hoechst 33342 (синий). Сверху вниз: неполяризованная неподвижная клетка демонстрирует ламеллу с активным раффлингом; клетка, движущаяся вниз вправо, демонстрирует активный блеббинг; клетка, движущаяся влево, — удлинение ламеллы. Все три клетки без выростов демонстрируют колокализацию окрашивания антителами к β-актину и фаллоидином на периферии цитоплазмы, то есть в зонах ламеллярных расширений с раффлингом/блеббингом, при этом отсутствует колокализация в центральной области. В нижней панели клетка с выростами демонстрирует частичную колокализацию окрашивания антителами с фаллоидином и содержит актиновые глобулы как в соме клетки, так и в выростах.
Для изучения потенциальной роли дивергентного актина HdA6 в структурной организации губки H. dujardinii авторы провели секвенирование единичных клеток губки (scRNA-seq) с двумя независимыми биологическими повторностями. В результате секвенирования единичных клеток (scRNA-seq) был выявлен 21 уникальный кластер с характерными маркерами у 22 145 отдельных клеток. Проведён интеграционный анализ scRNA-seq и bulk RNA-seq данных, включая образцы, собранные в разные сезоны. Показано, что некоторые дифференциально экспрессируемые гены определяют не только отдельные кластеры, но и группы кластеров, что указывает на иерархическую организацию клеточных линий у губки. Наиболее многочисленными оказались кластеры CL0 и CL2, образующие центральный массив клеток (Рис. 3A). Кластер 0 содержит наибольшее число клеток и экспрессирует гены, связанные с регуляцией внеклеточного матрикса. Кластер 2 дополнительно экспрессирует гены, связанные с пролиферацией клеток, он представляет собой пролиферирующую разновидность клеток кластера 0. Для идентификации клеточных типов был использован метод SAMap (self-assembled manifold mapping), который позволил сравнить кластеры H. dujardinii с аннотированными клеточными типами из других видов губок: ювенильной пресноводной губки Spongilla lacustris и морской губки Amphimedon queenslandica [6, 7]. Кластер 0 был сопоставлен с несколькими типами клеток, включая хоаноциты и археоциты. Консервативные актины HdA1/2/3 равномерно экспрессируются во всех кластерах, но дивергентный актин HdA6 демонстрирует специфичную экспрессию в трёх кластерах: 3, 5 и 8 (Рис. 3Б, В).
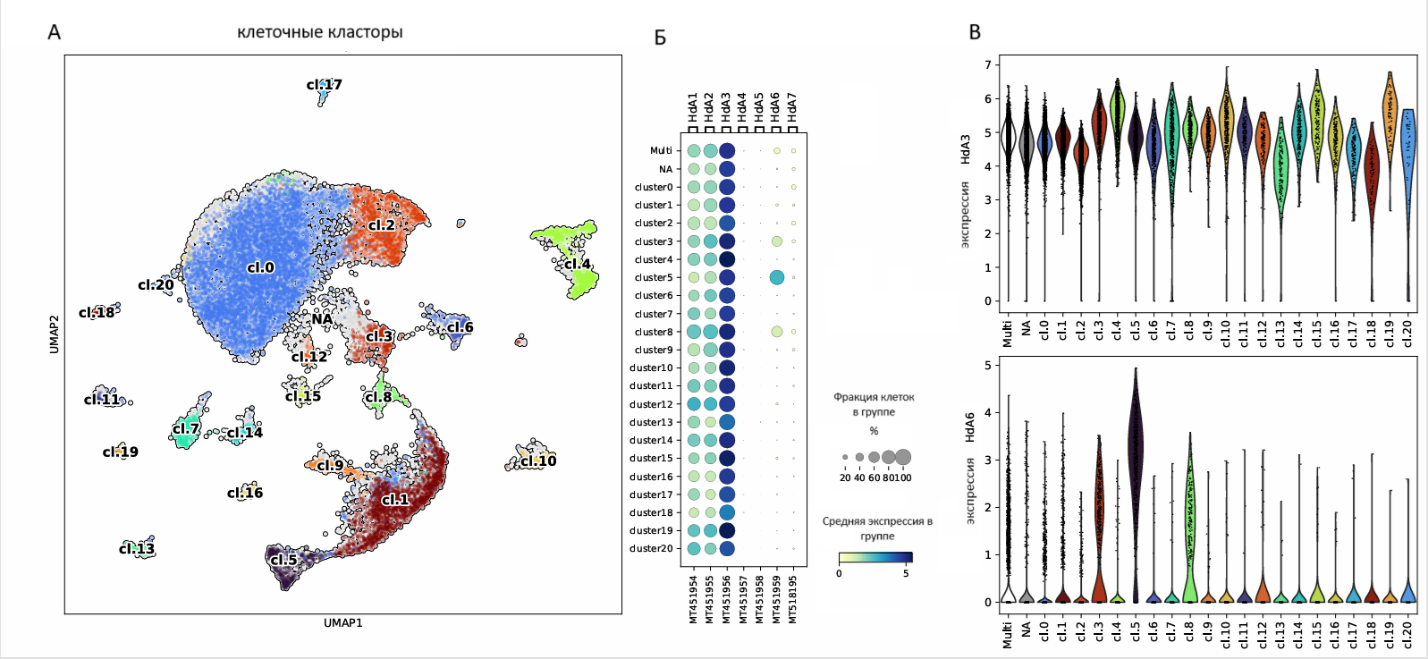
Рис. 3. Анализ клеточного состава морской губки H. dujardinii на основе РНК-секвенирования единичных клеток (Sc RNAseq).
(А) UMAP-проекция клеток H. dujardinii после рекластеризации на 21 кластер, каждый из которых определён на основе наборов маркерных генов; клетки, экспрессирующие несколько маркерных генов или не экспрессирующие ни один, показаны бледно-серым цветом.
(Б) Dotplot, иллюстрирующий экспрессию генов актина в различных клеточных кластерах. Цвет отражает среднее значение количества прочтений данного гена в конкретном кластере. Размер точек показывает долю клеток с ненулевым уровнем экспрессии этого гена.
(В) Скрипичные плоты, демонстрирующие распределение уровней экспрессии актинов в каждом клеточном кластере для HdA3 (как представителя повсеместно экспрессируемых консервативных паралогов актина) и HdA6.
Для выявления связи клеточной специфичности с процессом реагрегации клеток губки, авторы провели интеграцию данных секвенирования единичных клеток (scRNA-seq) и транскриптомного анализа RNA-seq (bulk RNA-seq). Анализ охватывал образцы на разных стадиях: диссоциированные клетки, клеточные агрегаты и интактные ткани. Bulk-анализ также позволил учитывать сезонные колебания экспрессии генов.
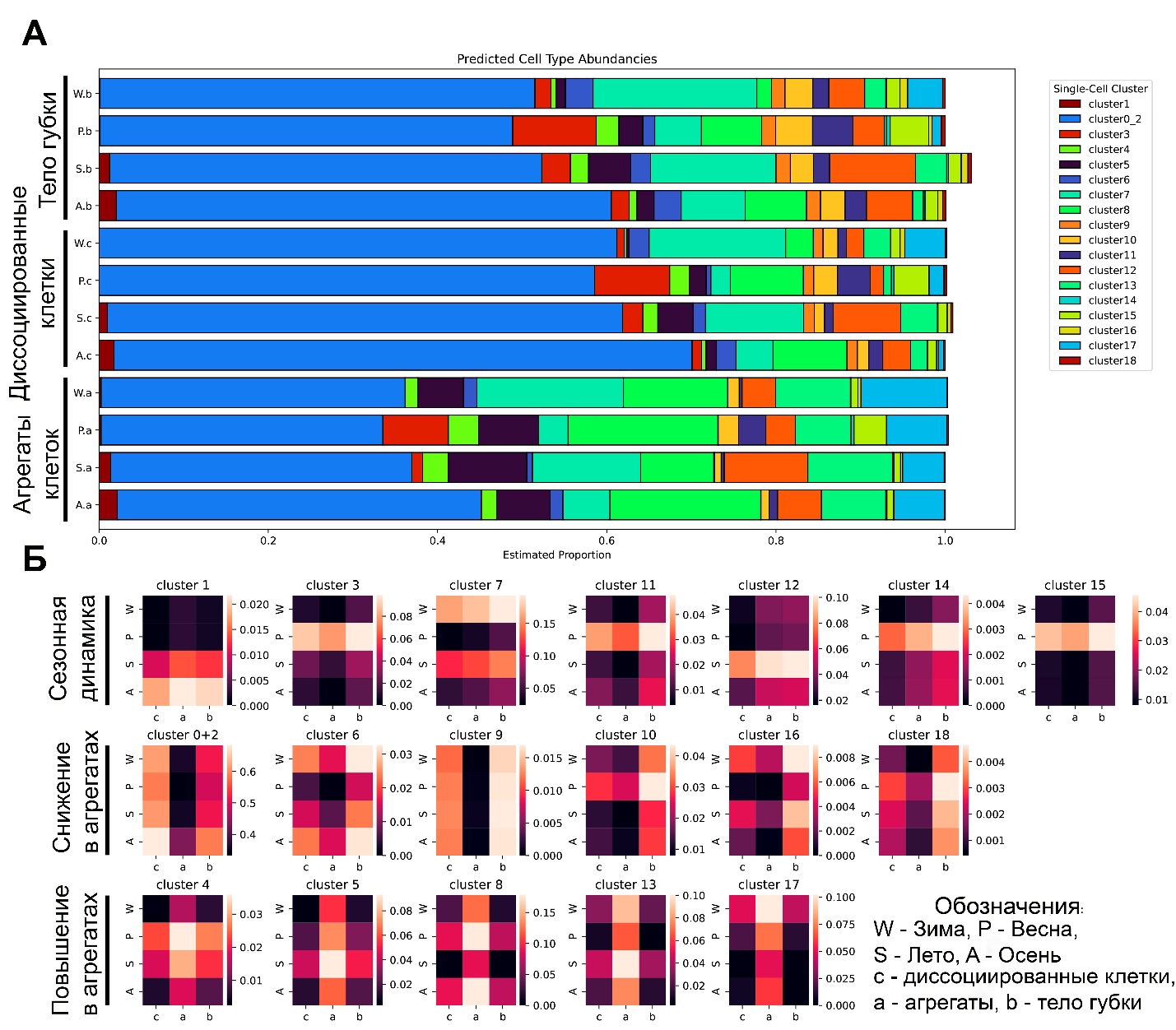
Рис. 4. Анализ деконволюции клеточных типов морской губки H. dujardinii.
(А) Деконволюция типов клеток в образцах bulk RNA-seq с использованием MuSiC, при этом кластеры 0 и 2 объединены из-за схожих паттернов экспрессии генов и нестабильных прогнозов по пропорциям, а кластеры 19 и 20 исключены из-за недостаточной стабильности маркерных генов. Результаты повторов объединены с помощью смешанного линейного моделирования в lme4.
(Б) Данные того же анализа представлены в виде отдельных тепловых карт по каждому кластеру, что позволяет выделить три основных паттерна: только сезонная динамика, истощение на стадии агрегации и обогащение на стадии агрегации.
Динамика клеточных популяций в процессах механической диссоциации и реагрегации клеток в агрегаты представлена на рис. 4. Установлено, что при диссоциации тела губки уменьшается численность кластера 5 (экспрессирующего HdA6), но увеличивается количество в кластерах 0 и 2 (экспрессирующих HdA1/2/3). При реагрегации клеток наблюдается противоположная картина: клетки кластера 5 становятся доминирующими. Очевидно, экспрессия HdA6 играет уникальную роль в адаптации к механическому стрессу и реагрегации клеток. Анализ экспрессии сигнальных путей регуляции актинового цитоскелета показал их клеточную специфичность у губок. RhoA-, Hippo/YAP- и Wnt/Frizzled- сигнальные пути активируются при реагрегации: RhoA- и Hippo/YAP-пути регулируют адгезию, Wnt/Frizzled-сигнализация участвует в установлении новых межклеточных контактов, а EGFR-зависимый путь, является ключевым в агрегирующих клетках, экспрессирующих дивергентный актин HdA6.
Таким образом, клеточные типы губок сочетают черты примитивного и продвинутого уровня организации актинового цитоскелета, что делает их особенно интересными для изучения его эволюции. Молекулярные механизмы, регулирующие актиновый цитоскелет, наличие функционально дивергентного актина в определенных клеточных типах и снижение его в период реагрегации, способствуют сохранению клеточного потенциала внутри агрегатов, необходимого для последующих трансформаций в новый целостный организм. Интересно, что такой подход применяют при культивировании индуцированных плюрипотентных стволовых клеток млекопитающих для поддержания их жизнеспособности и плюрипотентности: в культуральную среду добавляют ингибитор ROCK (Rho-ассоциированной протеинкиназы) Y-27632, который подавляет динамику актинового цитоскелета. Дальнейшее выявление уникальных механизмов ремоделлинга актинового цитоскелета у базальных многоклеточных представляет собой интригующую задачу для исследователей. Данные могут быть использованы в биоинженерии, где необходимо воспроизводить точную клеточную перестройку для самосборки тканей.
Список литературы:
1. Wilson HV The behaviour of the dissociated cells in hydroids, Alcyonaria, and Asterias. J Exp Zool. 1911; 11:281–338. 10.1002/jez.1400110304.
2. Vedula P, Kurosaka S, Leu NA et al. Diverse functions of homologous actin isoforms are defined by their nucleotide, rather than their amino acid sequence. eLife. 2017; 6:e31661.
3. Vedula P, Kurosaka S, MacTaggart B et al. Different translation dynamics of β- and γ-actin regulates cell migration. eLife. 2021; 10:e68712. 10.7554/eLife.68712.
4. Bagavathi S, Malathi R Introns and protein revolution — an analysis of the exon/intron organisation of actin genes. FEBS Lett. 1996; 392:63–5. 10.1016/0014-5793(96)00769-7.
Новость подготовили
© Люпина Ю.В.Главный научный сотрудник. Доктор биологических наук.
Кравчук О.И., Ведущий научный сотрудник. Кандидат биологических наук.
04.12.2025